题目内容
18.下列说法正确的是( )| A. | 8g碳和14g氧气反应生成22g二氧化碳 | |
| B. | 二氧化碳由一个碳原子和两个氧原子构成 | |
| C. | 1g硫和1g氧气反应生成2g二氧化硫 | |
| D. | 水银温度计在温度升高时水银柱上升是因为汞原子的体积变大 |
分析 A、根据碳和氧气反应时的质量比为3:8来计算;
B、二氧化碳的分子式为CO2;
C.在S的燃烧反应中,S、O2和生成的SO2的质量之比为1:1:2;
D.原子的体积不会随着温度的改变而改变,温度改变的是原子间的距离.
解答 解:A、碳和氧气反应时的质量比为3:8,故8g碳和14g氧气反应时碳过量,碳没有完全反应,故生成的二氧化碳的质量小于22g,故A错误;
B、根据二氧化碳的分子式可知,二氧化碳由一个碳原子和两个氧原子构成,故B正确;
C.该反应中反应物和生成物的质量比为32:(16×2):(32+16×2)=1:1:2,故C正确;
D.原子间有间隔,间隔的大小随温度的改变而改变,原子的大小没有改变,故D错误.
故选BC.
点评 本题考查了物质的构成和反应时量的关系,熟知化学式的宏观和微观意义是解答此类试题的关键.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
9.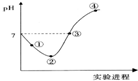 常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol•L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是( )
常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol•L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是( )
 常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol•L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是( )
常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol•L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是( )| A. | ②点之前所发生反应的离子方程式为Cl2+H2O=2H++Cl-+ClO- | |
| B. | ③点所示溶液中:c(Na+)=c(Cl-)+c(ClO-) | |
| C. | 实验进程中溶液的pH可以用pH试纸测得 | |
| D. | 曲线起点处水的电离程度最大 |
6.金秋十月,人们只要靠近盛开桂花的桂花树时,就能闻到怡人的桂花香.其原因是( )
| A. | 微粒体积很小 | B. | 微粒之间有间隔 | ||
| C. | 微粒质量很小 | D. | 微粒在不停的运动 |
13.元素X原子最外层上有3个电子,元素Y最外层上有6个电子,由X、Y两种元素形成的化合物的化学式可能为( )
| A. | XY | B. | X2Y3 | C. | XY2 | D. | X2Y |
7.乙烯产量是衡量一个国家石油化工发展水平的标志.下列关于乙烯说法正确的是( )
| A. | 与乙烷互为同分异构体 | B. | 分子中存在C≡C | ||
| C. | 能使酸性高锰酸钾溶液褪色 | D. | 分子中存在C=O |
8.有机分子中,当某个碳原子连接着四个不同的原子或原子团时,这种碳原子称为“手性碳原子”.例如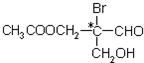 是某有机物分子的结构简式,其中带“*”的碳原子就是手性碳原子.当此有机物分别发生下列反应后,生成的有机物分子中仍含有手性碳原子的是( )
是某有机物分子的结构简式,其中带“*”的碳原子就是手性碳原子.当此有机物分别发生下列反应后,生成的有机物分子中仍含有手性碳原子的是( )
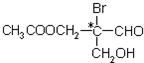 是某有机物分子的结构简式,其中带“*”的碳原子就是手性碳原子.当此有机物分别发生下列反应后,生成的有机物分子中仍含有手性碳原子的是( )
是某有机物分子的结构简式,其中带“*”的碳原子就是手性碳原子.当此有机物分别发生下列反应后,生成的有机物分子中仍含有手性碳原子的是( )| A. | 与乙酸发生酯化反应 | B. | 与NaOH水溶液反应 | ||
| C. | 催化剂作用下与H2反应 | D. | 与银氨溶液作用发生银镜反应 |
 Ω=2,则有机物
Ω=2,则有机物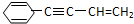 的不饱和度为( )
的不饱和度为( )