题目内容
18.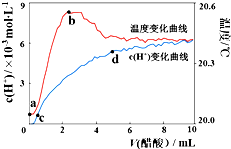 室温下,将10.00mL 5.0000mol•L-1醋酸滴入100.00mL蒸馏水中,溶液中c(H+)和温度随着醋酸体积变化曲线如图所示.下列有关说法正确的是( )
室温下,将10.00mL 5.0000mol•L-1醋酸滴入100.00mL蒸馏水中,溶液中c(H+)和温度随着醋酸体积变化曲线如图所示.下列有关说法正确的是( )| A. | a~b段,醋酸电离过程为放热过程 | |
| B. | c~d段,c(H+)增加,醋酸电离度增加 | |
| C. | c点时,加入等体积等浓度的NaOH溶液则:c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| D. | d点时,c(H+)>c(CH3COOH) |
分析 醋酸溶于水时,既有醋酸的电离又有氢离子和醋酸根离子的水和,醋酸电离过程为吸热过程,氢离子和醋酸根离子的水合过程(形成水合离子)放热,醋酸浓度越低,其电离度越大,但醋酸的电离程度很小,据此分析.
解答 解:A、a~b段,醋酸电离过程为吸热过程,电解质溶于水,扩散过程(电离)吸热,水合过程(形成水合离子)放热,故A错误;
B、c~d段,醋酸浓度增大,c(H+)增加,醋酸电离程度减小,越稀越电离,故B错误;
C、c点时,加入等体积等浓度的NaOH溶液,根据物料守恒,有c(Na+)=c(CH3COO-)+c(CH3COOH),故C正确;
D、d点时,c(H+)<c(CH3COOH),故D错误;
故选C.
点评 本题考查了弱电解质醋酸电离过程中的能量变化和离子浓度变化,注意醋酸溶于水时,既有醋酸的电离又有氢离子和醋酸根离子的水和,醋酸电离过程为吸热过程,氢离子和醋酸根离子的水合过程(形成水合离子)放热,题目难度不大.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案
相关题目
8.设NA表示阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 常温常压下,2.8gN2与C2H4的混合气体中含有的电子数为1.4NA | |
| B. | 标准状况下,1.12L NO与1.12LO2的混合物中含有的原子数为0.2NA | |
| C. | 25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA | |
| D. | 常温下,1L0.1mol•L-1的NH4NO3溶液中氧原子数为0.3NA |
9.下列说法正确的是( )
| A. | 常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)能自发进行,证明该反应的△H<0 | |
| B. | 常温下,BaSO4分别在相同物质的量浓度的Na2SO4溶液和Al2(SO4)3溶液中的溶解度相同 | |
| C. | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,说明常温下Ksp(BaCO3)<Ksp(BaSO4) | |
| D. | 等体积、等物质的量浓度的NH3•H2O溶液与NH4Cl溶液混合后溶液呈碱性,说明NH3•H2O的电离程度小于NH${\;}_{4}^{+}$的水解程度 |
6.在固定容积的密闭容器中,可逆反应2X(g)+2Y(s)?3Z(g),达到平衡后,若将容器中X、Y、Z的物质的量均减少一半,对该反应产生的影响是( )
| A. | 正、逆反应速率都减小,平衡不移动 | |
| B. | 正、逆反应速率都减小,平衡向正反应方向移动 | |
| C. | 正反应速率增大,逆反应速率减小,平衡向正反应方向移动 | |
| D. | 正反应速率减小,逆反应速率增大,平衡向逆反应方向移动 |
13.已知温度T时KW=1.0×10-12,0.1mol/L Na2A溶液pH=6,则下列说法中,正确的是( )
| A. | 该温度下,0.005mol/L H2A溶液中水电离出的c(H+)=10-12mol/L | |
| B. | H2A在水溶液中的电离方程式为:H2A?H++HA-,HA-?A2-+H+ | |
| C. | (NH4)2A溶液中存在离子浓度关系:(NH4+)>(A2-)>(H+)>(OH-) | |
| D. | 等体积等浓度的盐酸与H2A溶液分别与5.6gFe反应,H2A产生的H2多 |
3.NA表示阿伙加德罗常数的值.下列判断正确的是( )
| A. | 常温常压下,17g氨气分子所含质子数为10NA | |
| B. | 1mol CL2参加反应,转移电子数一定为2N | |
| C. | 常温常压下,22.4 L C02分子中含有2NA个σ键和2NA个1π键 | |
| D. | 1 L 0.01 mol.L-1的Na2CO3溶液中含有0.01NA个CO2- |
9.某元素R的最高价氧化物的化学式为RO2,其气态氢化物中氢的质量分数为25%,此元素是( )
| A. | C | B. | N | C. | Si | D. | S |