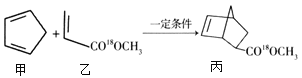题目内容
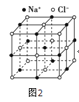
【题目】已知某离子晶体的晶胞如图所示,其摩尔质量为Mg/mol,阿伏加德罗常数的值为NA,晶体的密度为dg/cm9。下列关于该晶体的说法正确的是( )
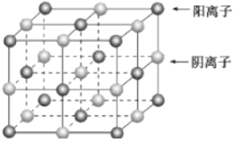
A.晶胞中阴、阳离子的个数都为1
B.阴、阳离子的配位数都是4
C.该晶胞可能是NaCl的晶胞
D.该晶体中两个距离最近的阳离子的核间距为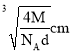
【答案】C
【解析】
A.R位于晶胞顶点及面心,R的数目为![]() ,L位于晶胞棱及体心,L的数目为
,L位于晶胞棱及体心,L的数目为![]() ,A项错误;
,A项错误;
B.根据晶胞结构图可知,R、L的配位数均为6,B项错误;
C.该晶胞中阴、阳离子个数比为1:1,故可能是NaCl晶胞,C选项正确;
D.设该晶胞边长为a cm,两个距离最近的阳离子的核间距相当于晶胞中某一面对角线的一半,即为![]() ,晶胞中含有4个R和4个L则晶胞的质量为
,晶胞中含有4个R和4个L则晶胞的质量为![]() ,所以晶体的密度为
,所以晶体的密度为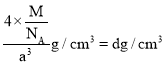 ,所以
,所以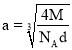 ,两个距离最近的阳离子的核间距为
,两个距离最近的阳离子的核间距为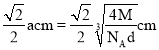 ,D项错误;
,D项错误;
答案选C。

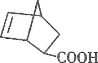
【题目】利用铜萃取剂M,通过如下反应实现铜离子的富集:

(1)X难溶于水、易溶于有机溶剂,其晶体类型为________。
(2)M所含元素的电负性由大到小顺序为_______,N原子以_____轨道与O原子形成σ键。
(3)上述反应中断裂和生成的化学键有______(填序号)。
a.离子键
b.配位键
c.金属键
d.范德华力
e.共价键
(4)M与W(分子结构如图)相比,M的水溶性小,更利于Cu2+的萃取。M水溶性小的主要原因是_____。

(5)基态Cu2+的外围电子排布式为________,Cu2+等过渡元素水合离子是否有颜色与原子结构有关,且存在一定的规律。判断Sc3+、Zn2+的水合离子为无色的依据是___________。
离子 | Sc3+ | Ti3+ | Fe2+ | Cu2+ | Zn2+ |
颜色 | 无色 | 紫红色 | 浅绿色 | 蓝色 | 无色 |
【题目】氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,某同学在实验室中对NH3与NOx反应进行了探究。回答下列问题:
(1)氨气的制备

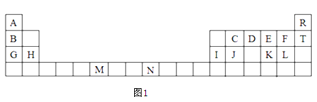
①氨气的发生装置可以选择上图中的________,反应的化学方程式为______________。
②预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→______(按气流方向,用小写字母表示)。
(2)氨气与二氧化氮的反应将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。

操作步骤 | 实验现象 | 解释原因 |
打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中 | ①Y管中_____________ | ②反应的化学方程式 ____________ |
将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝集 |
打开K2 | ③_______________ | ④______________ |
【题目】下图是古丝绸之路中的重要贸易商品,下列有关说法错误的是
|
|
|
|
瓷器 | 丝绸 | 茶叶 | 酒 |
A.陶瓷由黏土经高温烧结而成,其主要成分是硅酸盐
B.丝绸的化学成分主要是纤维素,纤维素属于天然有机高分子化合物
C.茶叶中含多种酚类物质,经常饮用可抗氧化、防衰老
D.我国劳动人民很早就掌握了酿酒技术,但自酿酒中可能会含有甲醇等有害物质,不建议直接饮用