题目内容
【题目】通常检测SO2含量是否达到排放标准的反应原理是SO2 +H2O2 + BaCl2 ===BaSO4↓+ 2HCl。NA表示阿伏伽德罗常数,下列说法正确的是( )
A. 0.1 mol BaCl2晶体中所含微粒总数为0.1NA
B. 25 ℃时,pH =1的HCl溶液中含有H+的数目为0.1NA
C. 17 g H2O2中含有非极性键数目为0.5NA
D. 生成2.33 g BaSO4沉淀时,转移电子数目为0.01NA
【答案】C
【解析】A. 由钡离子和氯离子构成,故0.1molBaCl2晶体中所含微粒总数为0.3NA,选项A错误;B. 没有给定体积,无法计算H+的数目,选项B错误;C. H2O2的结构式为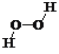 ,l7gH2O2为0.5mol,含有非极性键数目为0.5NA,选项C正确;D. 根据反应SO2+H2O2+BaCl2=BaSO4↓+2HCl,生成2.33gBaSO4沉淀(0.01mol)时,转移电子数目为0.02NA,选项D错误。答案选C。
,l7gH2O2为0.5mol,含有非极性键数目为0.5NA,选项C正确;D. 根据反应SO2+H2O2+BaCl2=BaSO4↓+2HCl,生成2.33gBaSO4沉淀(0.01mol)时,转移电子数目为0.02NA,选项D错误。答案选C。

【题目】已知 25℃时部分弱电解质的电离平衡常数数据如表:
化学式 | HSCN | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.3×10﹣1 | 1.8×10﹣5 | Ka1=4.3×10﹣1Ka2=5.6×10﹣1 | 3.0×10﹣8 |
回答下列问题:
(1)写出碳酸的主要的电离方程式 . 若将碳酸饱和溶液稀释 10 倍,则稀释后的溶液中 c(H+)原来的十分之一(填“大于”、“小于”或“等于”).
(2)物质的量浓度均为 0.1mol/L 的五种溶液:pH 由小到大的顺序为(用编号填写).
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3 e.NaSCN
(3)25℃时,将 20mL0.1molL﹣1CH COOH 溶液和 20mL0.1molL﹣1HSCN 溶液分别与 20mL0.1molL﹣1NaHCO 溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图.
反应初始阶段两种溶液产生 CO2气体的速率存在明显差异的原因是反应结束后,假设 NaHCO3完全反应且气体全部逸出,则所得两溶液中,c(CH3COO)c(SCN)(填“>”、“<”或“=”)
(4)25℃时,CH3COONa 与 CH3COOH 的混合溶液,若测得 pH=8,则溶液中c(Na+)﹣c(CH3COO﹣)=mol/L(填代入数据后的计算式,不必算出具体数值).
(5)向 NaClO 溶液中通入少量的 CO2 , 发生反应的离子方程式为 .
【题目】在2L密闭容器内,800℃时反应2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.006 | 0.006 | 0.006 |
(1)上述反应在第5s时NO的转化率是___________。用O2表示从0~2s内该反应的平均速率V(O2)=__________。
(2)下图中表示NO2的变化的曲线是__________。

(3)能使该反应的反应速率增大的是__________。
A.及时分离出NO2气体 B.适当升高温度 C.增大O2的浓度 D.选择高效催化剂
(4)能说明该反应已达到平衡状态的是___________。
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v逆(NO)=2v正(O2) D.容器内质量保持不变