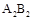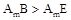题目内容
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在短周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料。下列说法中正确的是( )
A.元素A、B组成的化合物常温下一定呈气态
B.工业上常用电解法制备元素C、D、E的单质
C.离子半径:C>D>E
D.最高价氧化物对应水化物的碱性:C<D
B
解析试题分析:B原子最外层电子数是其电子层数的2倍,则B为C;A原子序数小于B,且单质在常温下是气体,则A为H; C在短周期的主族元素中原子半径最大,则C为Na; D的合金是日常生活中常用的金属材料,则D为Al;E原子序数大于Al,且单质在常温下是气体,则E为Cl。C、H组成的有机物常温下不一定是气态,A错;Na、Al、Cl2的在工业上常用电解法制取,B正确;电子层相同时,核电荷数越大,离子半径越小,因此离子半径Cl->Na+>Al3+,C错;NaOH是强碱,Al(OH)3是两性氢氧化物,因此碱性NaOH> Al(OH)3,D错。
考点:考查元素周期律,元素周期表,元素化合物性质。

练习册系列答案
相关题目
据报道,每百吨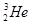 核聚变所释放出的能量相当于目前人类一年消耗的能量,在地球上氦元素主要以
核聚变所释放出的能量相当于目前人类一年消耗的能量,在地球上氦元素主要以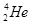 的形式存在。有关该元素说法正确的是
的形式存在。有关该元素说法正确的是
A.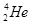 原子核内有4个质子 原子核内有4个质子 |
B.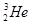 和 和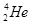 互为同位素 互为同位素 |
C.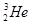 原子核内有3个中子 原子核内有3个中子 |
D.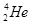 最外层只有2个电子故具有较强的金属性 最外层只有2个电子故具有较强的金属性 |
下图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是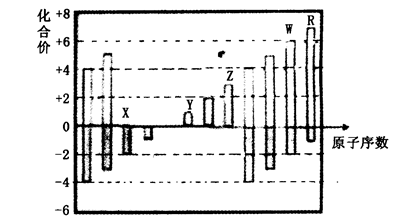
| A.原子半径:Z>Y>X |
| B.气态氢化物的稳定性:R<W |
| C.WX3和水反应生成的化合物是离子化合物 |
| D.Y和Z两者最高价氧化物对应的水化物能相互反应 |
短周期元素T、X、Y、Z的原子序数依次增大,T与Z属于同一主族,X、Y、Z最高价氧化物对应的水化物两两之间都能反应,且X、Y、Z原子最外层电子数之和等于X的原子序数。则下列说法正确的是
| A.简单离子半径大小顺序:rT>rX>rY |
| B.T与Z的最高正化合价相等 |
| C.室温下,单质Y不能与浓硫酸反应 |
| D.用电解法可制得T、X、Y的单质 |
下列说法正确的是
A.H与D,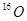 与 与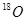 互为同位素: 互为同位素: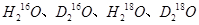 互为同素异形体 互为同素异形体 |
| B.元素X含氧酸的酸性强于元素Y的含氧酸的酸性,则X的得电子能力强于元素Y |
| C.质量数相同的不同核素,一定属于不同种元素 |
D.常温下,在pH=1的溶液中,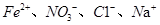 能够大量共存 能够大量共存 |
有四组同族元素的物质,在101.3KPa时测定它们的沸点(0C)如下表所示:
| 第一组 | He -268.8 | (a) -249.5 | Ar -185.8 | Kr -151.7 |
| 第二组 | F2 -187.0 | Cl2 -33.6 | (b) 58.7 | I2 184.0 |
| 第三组 | (c) 19.4 | HCl -84.0 | HBr -67.0 | HI -35.3 |
| 第四组 | H2O 100.0 | H2S -60.2 | (d) -42.0 | H2Te -1.8 |
下列各项中正确的是
A.a、b、c的化学式分别为Ne2、Br2、HF
B.第二组物质只表现氧化性,不表现还原性
C.第三组物质中C的沸点最高,是因为c分子量最大
D.第四组中各化合物的稳定性顺序为:H2O>H2S>H2Se>H2Te