题目内容
把0.6 mol气体X和0.4mol气体Y混合于2L容器中,使其发生如下反应:3X (g)+ Y(g) 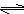 nZ (g) + 2W (g),5min末生成0.2 mol W,若测得以Z浓度变化表示的平均反应速率为0.01 mol·(L·min)-1,则n的值为( )
nZ (g) + 2W (g),5min末生成0.2 mol W,若测得以Z浓度变化表示的平均反应速率为0.01 mol·(L·min)-1,则n的值为( )
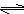 nZ (g) + 2W (g),5min末生成0.2 mol W,若测得以Z浓度变化表示的平均反应速率为0.01 mol·(L·min)-1,则n的值为( )
nZ (g) + 2W (g),5min末生成0.2 mol W,若测得以Z浓度变化表示的平均反应速率为0.01 mol·(L·min)-1,则n的值为( )| A.1 | B.2 | C.3 | D.4 |
A
略

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 P(g)+Q(g) ΔH>0,
P(g)+Q(g) ΔH>0, 
 CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol, 测
CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol, 测 2NH3;△H<0达到平衡后,改变条件建立的新平衡(图中横坐标表示反应时间, 纵坐标表示反应速率)
2NH3;△H<0达到平衡后,改变条件建立的新平衡(图中横坐标表示反应时间, 纵坐标表示反应速率) 

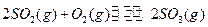
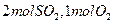 ,达平衡时生成
,达平衡时生成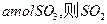 的转化率为 。
的转化率为 。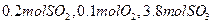 ,达平衡时SO2的物质的量为 mol。
,达平衡时SO2的物质的量为 mol。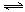 CO(g) + H2(g)
CO(g) + H2(g)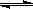 pC(气)+qD(气),若增大压强,或升高温度,重新达到平衡,
pC(气)+qD(气),若增大压强,或升高温度,重新达到平衡, 随时间化过程均如图所示,则对该反应叙述正确的是( )
随时间化过程均如图所示,则对该反应叙述正确的是( ) 
 2C(g),在反应过程中体系的温度持续升高,实验测得混合气体中C的含量与温度关系如图所示。下列说法正确的是
2C(g),在反应过程中体系的温度持续升高,实验测得混合气体中C的含量与温度关系如图所示。下列说法正确的是