��Ŀ����
����Ŀ������ij��������ɫ����Һ�����ܺ������������е������֣�
Na����NH4����Cl����Mg2����Ba2����CO32����SO42������ȡ���ݸ�100mL��Һ��������ʵ�飺
����һ�ݼ�������AgNO3��Һ�г���������������ϡ�������������ܽ⣻
���ڶ��ݼ�����NaOH��Һ��ּ��Ⱥ��ռ�������0.896L(��״��)��
�������ݼ�����BaCl2��Һ���˺��ָ���õ�����6.27g���پ�����ϡ����ϴ�ӡ��������������Ϊ2.33g����������ʵ��������й����ݣ��ش��������⣺
��1��ԭ��Һ��һ�����ڵ��������� ��һ�������ڵ������� �����ܴ��ڵ������� ��
��2�����з�����ѧ��Ӧ�����ӷ���ʽΪ ��
��3���������ɿ�����ϡ����ij�����ѧʽΪ �����ʵ���Ϊ mol,�ó�������ϡ��������ӷ���ʽΪ ��
���𰸡�(1)CO32����SO42��;Mg2����Ba2��; Cl-
(2)NH4��+OH-![]() NH3��+H2O
NH3��+H2O
(3)BaCO3��0.02��BaCO3+2H+=Ba2++CO2��+H2O
�����������������������AgNO3��Һ���г������ɣ������������������ʧ����Һ�к���Cl����CO32����SO42�����ٺ���һ�֣�����������������Һ�����Ȳ������壬������Ϊ��������Һ�к���NH4���������ʵ���Ϊ0.896/22.4mol=0.04mol��������BaCl2�õ�������������������������٣�һ������CO32����SO42�����������ӹ��棬һ��û��Mg2����Ba2���������������n(SO42��)=2.33/233mol=0.01mol��n(CO32��)=(6.27��2.33)/197mol=0.02mol��������Һ���ֵ����ԣ�����������������ʵ���Ϊ0.04mol������������������ʵ���0.06mol����˺���һ������Na������1�� CO32����SO42����Mg2����Ba2���� Cl-����2�� NH4����OH��![]() NH3����H2O��3��BaCO3��0.02 ��BaCO3+2H+=Ba2++CO2��+H2O��
NH3����H2O��3��BaCO3��0.02 ��BaCO3+2H+=Ba2++CO2��+H2O��

 �߽�������ϵ�д�
�߽�������ϵ�д�����Ŀ��ij�о���С��̽�����������ķ�Ӧ������ʵ�����£�
CH3COOH + C2H5OH ![]() CH3COOC2H5 + H2O
CH3COOC2H5 + H2O
Ͷ�� 1 �� 1 CH3COOHת���� 65%
1 �� 10 CH3COOHת���� 97%
(��120 ���²ⶨ)
��֪������������ʣ����³�ѹ��
�ܶ�g/mL | �۵�/�� | �е�/�� | ˮ���� | |
�Ҵ� | 0.79 | -114 | 78 | �� |
���� | 1.049 | 16.2 | 117 | �� |
�������� | 0.902 | 84 | 76.5 | ���� |
�ϳɷ�Ӧ��
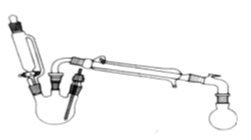
������ƿ�м����Ҵ�5 mL������5 mL��2СƬ���Ƭ��©����������14.3 mL ���Ҵ�20 mL����������ͨ����ȴˮ��ʼ�������ȣ����Ƶμ��ٶȵ��������ٶȣ���Ӧ�¶Ȳ�����120 �档
�����ᴿ��
����Ӧ�ֲ��ﵹ���Һ©���У��������������͵�Na2CO3��Һ������NaCl��Һ������CaCl2��Һϴ�ӣ�����������ˮ̼��أ�����һ��ʱ�����ȥ̼��ء�����ͨ������õ�����������������
�ش��������⣺
��1��������Ӧ�Ļ���
���Ҵ��ǻ���ʾ��
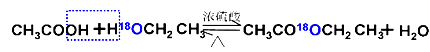
�ô����ǻ���ʾ��

����18ˮռ����ˮ����һ�룬��Ҳһ�������ʵ���Ʒ���������ӦΪ��ȡ����Ӧ����������������Ӧ�Ļ��� ��
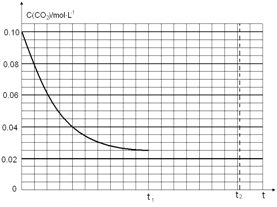
2��������Ӧ��һ������ķ�Ӧ��120 ��ʱ��ƽ�ⳣ��K= ��
��3���������һ��ʱ��������ǼӴ�Ƭ��Ӧ�ò�ȡ����ȷ������________(����ȷ�𰸱��)��
A���������� B����ȴ�� C�����貹�� D����������
��4��Ũ�������Ҵ���λ�ϣ� ��
��5�����Ƶμ�������Ҵ����Һ���ٶȵ��������ٶ�Ŀ���ǣ� ��
��6�������Ĵ�������������Ҫ����Щ���ʣ� �����͵�Na2CO3��Һϴ�ӳ�ȥ���ᡣ����ж��Ƿ������ ���ñ���NaCl��Һϴ�ӳ�ȥ������Na2CO3��Һ��Ϊʲô����ˮ�� ��