题目内容
下表为元素周期表的一部分,表中列出11种元素在周期表中的位置,按要求回答下列各题.
(1)这11种元素中,化学性质最不活泼的元素是______(用元素符号或化学式表示,下同),得电子能力最强的原子对应的单质是______,失电子能力最强的原子对应的单质与水反应的化学方程式是______.常温下为液态的非金属单质是______.
(2)元素④的离子结构示意图为

;
(3)⑥、⑦、⑧气态氢化物的化学式分别为______、______、______,其中以______最稳定.⑦、⑨两种元素最高价氧化物对应水化物的化学式分别为:______、______;其中以______酸性最强.
(4)③和⑨两种元素形成的化合物属于______(填“离子化合物”或“共价化合物”),请用电子式表示其形成过程______.
(5)写出③的单质置换出⑥的单质的化学方程式______.
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑧ | ⑩ | |||||
| 3 | ① | ③ | ⑤ | ⑦ | ⑨ | |||
| 4 | ② | ④ |
(2)元素④的离子结构示意图为

;
(3)⑥、⑦、⑧气态氢化物的化学式分别为______、______、______,其中以______最稳定.⑦、⑨两种元素最高价氧化物对应水化物的化学式分别为:______、______;其中以______酸性最强.
(4)③和⑨两种元素形成的化合物属于______(填“离子化合物”或“共价化合物”),请用电子式表示其形成过程______.
(5)写出③的单质置换出⑥的单质的化学方程式______.
根据元素在元素周期表中的位置可知,①为Na,②为K,③为Mg,④为Ca,⑤为Al,⑥为C,⑦为P,⑧为F,⑨为Cl,⑩为Ne,
(1)上述元素中只有Ne最外层电子数为8,为稳定结构,则化学性质最不活泼的元素Ne,上述元素中只有F的非金属性最强,则F2得电子能力最强,只有K的金属性最强,与水反应剧烈,该反应为2K+2H2O=2KOH+H2↑,溴单质在常温下为液体,其化学式为Br2,故答案为:Ne;F2;2K+2H2O=2KOH+H2↑;Br2;
(2)Ca的质子数为20,易失去最外层2个电子变为钙离子,离子结构示意图为

,故答案为:

;
(3)⑥为C,⑦为P,⑧为F,氢化物分别为CH4、PH3、HF,F非金属性最强,则HF越稳定;非金属性Cl>P,则元素最高价氧化物对应水化物分别为HClO4、H3PO4,HClO4的酸性强,
故答案为:CH4;PH3;HF;HF;H3PO4;HClO4;HClO4;
(4)Mg与Cl形成离子化合物为氯化镁,用电子式表示其形成过程为
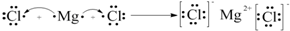
,
故答案为:离子化合物;
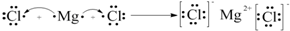
;
(5)镁与二氧化碳发生的置换反应为2Mg+CO2
2MgO+C,故答案为:2Mg+CO2
2MgO+C.
(1)上述元素中只有Ne最外层电子数为8,为稳定结构,则化学性质最不活泼的元素Ne,上述元素中只有F的非金属性最强,则F2得电子能力最强,只有K的金属性最强,与水反应剧烈,该反应为2K+2H2O=2KOH+H2↑,溴单质在常温下为液体,其化学式为Br2,故答案为:Ne;F2;2K+2H2O=2KOH+H2↑;Br2;
(2)Ca的质子数为20,易失去最外层2个电子变为钙离子,离子结构示意图为

,故答案为:

;
(3)⑥为C,⑦为P,⑧为F,氢化物分别为CH4、PH3、HF,F非金属性最强,则HF越稳定;非金属性Cl>P,则元素最高价氧化物对应水化物分别为HClO4、H3PO4,HClO4的酸性强,
故答案为:CH4;PH3;HF;HF;H3PO4;HClO4;HClO4;
(4)Mg与Cl形成离子化合物为氯化镁,用电子式表示其形成过程为
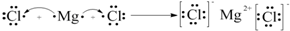
,
故答案为:离子化合物;
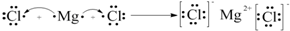
;
(5)镁与二氧化碳发生的置换反应为2Mg+CO2
| ||
| ||

练习册系列答案
相关题目








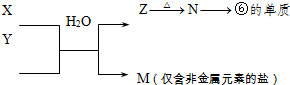
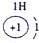
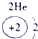
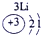
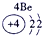
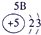
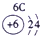
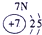
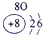
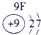
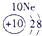
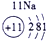





 表示的是
表示的是