题目内容
【题目】请按要求填空做答。
(1)NaHCO3能用于治疗胃酸过多,反应的离子方程式为_______。
(2)铁和水蒸气反应的化学方程式为3Fe+4H2O(g)![]() Fe3O4+4H2,该反应中84g Fe参加反应,转移电子的物质的量为__________。
Fe3O4+4H2,该反应中84g Fe参加反应,转移电子的物质的量为__________。
(3)制备Fe(OH)3的实验操作:向煮沸的蒸馏水中加入几滴FeCl3溶液,______。
(4)密度为1.84g/cm3,质量分数为98%的浓硫酸的物质的量浓度为________。
【答案】HCO3-+H+=CO2↑+H2O 4mol 继续煮沸,至溶液出现红褐色液体 18.4mol/L
【解析】
(1)NaHCO3治疗胃酸过多实际上是跟HCl反应,离子方程式为:HCO3-+H+=CO2↑+H2O,故答案为:HCO3-+H+=CO2↑+H2O;
(2)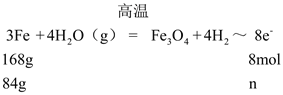 ,解得n= 4mol,故答案为:4mol;
,解得n= 4mol,故答案为:4mol;
(3)制备Fe(OH)3的实验操作:向煮沸的蒸馏水中加入几滴FeCl3溶液,继续煮沸,至溶液出现红褐色液体即制得氢氧化铁胶体,故答案为:继续煮沸,至溶液出现红褐色液体;
(4)由![]() 得:
得:![]() =18.4mol/L,故答案为:18.4mol/L。
=18.4mol/L,故答案为:18.4mol/L。

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目