题目内容
已知Zn(OH)2的溶度积常数为1.2×10-17 mol3/L3,则它在水中的溶解度为 ( )
| A.1.4×10-6 mol/L | B.2.3×10-6 mol/L |
| C.1.4×10-9 mol/L | D.2.3×10-9 mol/L |
A
此题主要是其溶解度是用物质的量浓度来表示的,在计算起来要容易一些。只需根据Zn(OH)2(s) Zn2+ (aq)+2OH-(aq),把握[Zn(OH)2]=[Zn2+]=0.5[OH-];再有其Ksp=[Zn2+]×[OH-]2,可先设[Zn2+]=a,则有a×(2a)2=1.2×10-17 mol3/L3,经计算可得[Zn(OH)2]=[Zn2+]=a=1.4×10-6 mol/L。
Zn2+ (aq)+2OH-(aq),把握[Zn(OH)2]=[Zn2+]=0.5[OH-];再有其Ksp=[Zn2+]×[OH-]2,可先设[Zn2+]=a,则有a×(2a)2=1.2×10-17 mol3/L3,经计算可得[Zn(OH)2]=[Zn2+]=a=1.4×10-6 mol/L。
 Zn2+ (aq)+2OH-(aq),把握[Zn(OH)2]=[Zn2+]=0.5[OH-];再有其Ksp=[Zn2+]×[OH-]2,可先设[Zn2+]=a,则有a×(2a)2=1.2×10-17 mol3/L3,经计算可得[Zn(OH)2]=[Zn2+]=a=1.4×10-6 mol/L。
Zn2+ (aq)+2OH-(aq),把握[Zn(OH)2]=[Zn2+]=0.5[OH-];再有其Ksp=[Zn2+]×[OH-]2,可先设[Zn2+]=a,则有a×(2a)2=1.2×10-17 mol3/L3,经计算可得[Zn(OH)2]=[Zn2+]=a=1.4×10-6 mol/L。
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
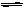 Ba2+(aq)+2OH-(aq)。向此种悬浊液中加入少量的氢氧化钡粉末,下列叙述正确的是 ( )
Ba2+(aq)+2OH-(aq)。向此种悬浊液中加入少量的氢氧化钡粉末,下列叙述正确的是 ( ) 一元弱酸HA(aq)中存在下列电离平衡:HA
一元弱酸HA(aq)中存在下列电离平衡:HA H++A-,如图将1.0 mol HA分子加入1.0 L水中,溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是
H++A-,如图将1.0 mol HA分子加入1.0 L水中,溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是