题目内容
6.非金属元素的原子间可形成离子化合物.如:NH4Cl、(NH4)2SO4、NH4HCO3等.分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,但非金属元素的原子之间可以形成离子键,如铵盐,据此分析解答.
解答 解:活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,但非金属元素的原子之间可以形成离子键,如铵盐NH4Cl、(NH4)2SO4、NH4HCO3等,故答案为:NH4Cl;(NH4)2SO4;NH4HCO3.
点评 本题考查离子化合物的判断,为高频考点,不能根据是否含有金属元素判断离子化合物,只含非金属元素的铵盐都是离子化合物,为易错点.

练习册系列答案
相关题目
17.下列实验操作不正确的是( )
| A. | 做过碘升华实验的烧杯用酒精洗涤 | |
| B. | 做过银镜反应实验的试管用稀硝酸洗涤 | |
| C. | 将汽油放在带橡皮塞的玻璃瓶中 | |
| D. | 往双氧水中滴入几滴三氯化铁溶液加快分解速率 |
14.下列各组离子能大量共存于同一溶液中的是( )
| A. | Na+、Fe2+、NO3-、H+ | B. | K+、Cu2+、NO3-、H+ | ||
| C. | H+、Na+、NO3-、HCO3- | D. | NH4+、Fe2+、NO3-、OH- |
11.将4mol A气体和2mol B气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)?2C(g),若经2s后测得C的浓度为0.6mol•L-1,现有下列几种说法正确的是( )
| A. | 用物质A表示的反应速率为0.3 mol/(L•s) | |
| B. | 用物质B表示的反应速率为0.6 mol/(L•s) | |
| C. | 2 s时物质A的转化率为70% | |
| D. | 2 s时物质B的浓度为0.7 mol•L-1 |
8.溶液中,下列电离方程式正确的是( )
| A. | KAl (SO4)2=K++Al3++2 SO42- | B. | H2CO3=H++HCO3- | ||
| C. | Ca(HCO3)2=Ca2++2H++2CO32- | D. | Ba(OH)2=Ba2++OH2- |
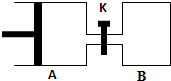 如图所示,容器A左侧是可平行移动的活塞.向A中充入1molX和1molY,向B中充入2molX和2molY,起始时V(A)=V(B)=aL.在相同温度和有催化剂存在的条件下,两容器各自发生:X(g)+Y(g)?Z(g)+2W(g),达到平衡时V(A)=1.2aL.试回答:
如图所示,容器A左侧是可平行移动的活塞.向A中充入1molX和1molY,向B中充入2molX和2molY,起始时V(A)=V(B)=aL.在相同温度和有催化剂存在的条件下,两容器各自发生:X(g)+Y(g)?Z(g)+2W(g),达到平衡时V(A)=1.2aL.试回答: