题目内容
【题目】标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω,物质浓度为c mol/L,则下列关系中不正确的是
A. ![]()
B. ![]()
C. ![]()
D. ![]() =1000Vρ/(17V+22400)
=1000Vρ/(17V+22400)
【答案】A
【解析】
A.将所给的式子的分子和分母同除以22.4可得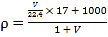 ,分子表示了溶液的质量,是合理的,但分母表达的是将溶剂的体积与气体的体积直接进行加和得到溶液的体积,这显然是错误的,A项错误;
,分子表示了溶液的质量,是合理的,但分母表达的是将溶剂的体积与气体的体积直接进行加和得到溶液的体积,这显然是错误的,A项错误;
B.假设取溶液的体积为1L,根据溶质质量分数的本义有:![]() ,分子表达了溶质质量,分母表达了溶液的质量,B项正确;
,分子表达了溶质质量,分母表达了溶液的质量,B项正确;
C.将所给的式子分子分母同除以22.4可得: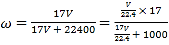 ,分子表达了溶质质量,分母表达了溶液的质量,C项正确;
,分子表达了溶质质量,分母表达了溶液的质量,C项正确;
D.将所给式子变形得: ,分子代表了溶质的物质的量,分母代表了溶液的体积(单位为L),D项正确;
,分子代表了溶质的物质的量,分母代表了溶液的体积(单位为L),D项正确;
所以答案选择A项。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目