题目内容
19.某质量数为32,核内有16个中子的原子,其电子排布式是1s22s22p63s23p4,该原子中有2个未成对电子,这些未成对电子具有相同(填“相同”或“相反”)的自旋状态.分析 质量数为32,核内有16个中子的原子,则质子数为32-16=16,为S元素的原子,核外有16个电子,未成对电子优先单独占据一个轨道自旋方向相同,以此来解答.
解答 解:质量数为32,核内有16个中子的原子,则质子数为32-16=16,为S元素的原子,其电子排布式为1s22s22p63s23p4,3p轨道上有2个未成对电子,这些未成对电子具有相同的自旋状态,故答案为:1s22s22p63s23p4;2;相同.
点评 本题考查原子的核外电子排布,为高频考点,把握质子数的计算及电子排布规律为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.根据下列反应的化学方程式判断下列物质氧化性强弱排序正确的是( )
①2FeCl3+Cu=2FeCl2+CuCl2 ②CuCl2+Fe=FeCl2+Cu.
①2FeCl3+Cu=2FeCl2+CuCl2 ②CuCl2+Fe=FeCl2+Cu.
| A. | CuCl2>FeCl2>FeCl3 | B. | FeCl3>FeCl2>CuCl2 | ||
| C. | CuCl2>FeCl3>FeCl2 | D. | FeCl3>CuCl2>FeCl2 |
10.下列有关化学用语表示正确的是( )
| A. | 12753I和12953I2互为同位素 | |
| B. | NH5的电子式为  | |
| C. | 氯原子的结构示意图: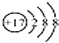 | |
| D. | 中子数为146、质子数为92的铀(U)原子14692U |
11.某气体的质量是同温、同压、同体积氢气质量的23倍,气体的相对分子质量是( )
| A. | 23 | B. | 46 | C. | 69 | D. | 92 |
8.下列有关实验室常用仪器和实验操作正确的是( )
| A. | 实验室用浓硫酸和乙醇制乙烯时,应把温度计的水银球靠近蒸馏烧瓶的支管口处 | |
| B. | 用浓硫酸配置一定物质的量浓度的稀硫酸时,应在量取浓硫酸后,用蒸馏水洗涤量筒并将洗涤液转移到小烧杯中 | |
| C. | 液态溴应贮存在磨口的细口瓶中,加水液封,加盖橡胶塞,并放置于阴凉处 | |
| D. | 应用渗析法提纯胶体时,要不断更换烧杯中的水(或用流动的水)以提高渗析效果 |
 .
.