题目内容
【题目】H2C2O4是一种二元弱酸。常温下向H2C2O4溶液中滴加KOH溶液,混合溶液中离子浓度与pH的关系如图所示,其中![]() 或
或![]() 。下列说法不正确的是
。下列说法不正确的是
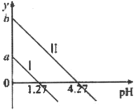
A.直线Ⅱ表示的是![]() 与pH的变化关系
与pH的变化关系
B.图中纵坐标应该是a=1.27,b=4.27
C.![]() 对应1.27<pH<4.27
对应1.27<pH<4.27
D.![]() 对应pH=7
对应pH=7
【答案】CD
【解析】
A.草酸为二元弱酸,一级电离抑制二级电离,电离常数![]() >
>![]() ,由图可知,当lgy=0时,溶液pH=-lgc(H+)=-lgK,pH1=1.27<pH2=4.27,表明K1=101.27>K2=104.27,所以直线I表示的是
,由图可知,当lgy=0时,溶液pH=-lgc(H+)=-lgK,pH1=1.27<pH2=4.27,表明K1=101.27>K2=104.27,所以直线I表示的是![]() 与pH的变化关系,直线Ⅱ表示的是
与pH的变化关系,直线Ⅱ表示的是![]() 与pH的变化关系,故A正确;
与pH的变化关系,故A正确;
B.由图可知,pH=0时,![]() =
=![]() ,
,![]() =
=![]() ,则图中纵坐标应该是a=1.27,b=4.27,故B正确;
,则图中纵坐标应该是a=1.27,b=4.27,故B正确;
C.设pH=a,c(H+)=10a,![]() =
=![]() ,
,![]() ,104.27-a>1,则4.27-a>0,解得a<4.27,
,104.27-a>1,则4.27-a>0,解得a<4.27,![]() =
=![]() ,
,![]() ,当
,当![]() ,102a-5.54>1,则2a-5.54>0,解得a>2.77,所以
,102a-5.54>1,则2a-5.54>0,解得a>2.77,所以![]() 对应2.77<pH<4.27,故C错误;
对应2.77<pH<4.27,故C错误;
D.由电荷守恒可得c(K+)+c(H+)=![]() +2
+2![]() +c(OH-),当c(K+)=
+c(OH-),当c(K+)=![]() +2
+2![]() 时,溶液中c(H+)=c(OH-), pH=7,故D错误;
时,溶液中c(H+)=c(OH-), pH=7,故D错误;
故选CD。

 名校课堂系列答案
名校课堂系列答案【题目】某矿渣的成分为Cu2O、Al2O3、Fe2O3、FeO、SiO2,工业上用该矿渣获取铜和胆矾的操作流程如图:

已知:①Cu2O+2H+=Cu+Cu2++H2O。
②部分阳离子以氢氧化物形式沉淀时溶液的pH如下表所示:
沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 5.4 | 4.0 | 2.7 | 5.8 |
沉淀完全pH | 6.7 | 5.2 | 3.7 | 8.8 |
(1)为了加快反应Ⅰ的速率,可以采取的措施是__(任写1条)。
(2)固体混合物A中的成分是__。
(3)反应Ⅰ完成后,铁元素的存在形式为__(填离子符号);检验该离子常用的方法之一是:取少量含该离子的溶液于试管中,滴加几滴铁氰化钾溶液,会产生沉淀,写出该反应的离子方程式__。
(4)操作1主要包括:__、__、__。洗涤CuSO4·5H2O粗产品不能用大量水洗,而用冰水洗涤。原因是__。
(5)用NaClO调pH可以生成沉淀B,利用题中所给信息分析沉淀B为__,该反应中氧化剂与还原剂的物质的量之比为__。
(6)用NaOH调pH可以生成沉淀C,利用题中所给信息分析y的范围为__。