题目内容
【题目】实验小组对SO2的性质进行探究。用如图所示装置进行实验。

(1)A的装置中浓硫酸的作用是___。
(2)请将A方框中的装置补充完整___。
(3)实验过程中,说明SO2与水反应生成了酸的实验现象是__。
(4)D的装置中发生反应的化学方程式为___。
【答案】吸收水蒸气(干燥SO2) 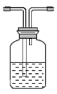 B中试纸不变色,C中试纸变红色 SO2+2NaOH=Na2SO3+H2O(SO2+NaOH=NaHSO3)
B中试纸不变色,C中试纸变红色 SO2+2NaOH=Na2SO3+H2O(SO2+NaOH=NaHSO3)
【解析】
根据实验装置图分析,装置A中的浓硫酸具有干燥的作用,SO2不能使干燥的蓝色石蕊试纸变色,但因为SO2与水反应生成亚硫酸,酸能使湿润的蓝色石蕊试纸变红,最后用氢氧化钠溶液进行尾气处理。
(1)SO2与浓硫酸不反应,浓硫酸有吸水性,可以吸收SO2中的水蒸气,所以浓硫酸的作用是吸收水蒸气(干燥SO2),故答案为:吸收水蒸气(干燥SO2);
(2)A的装置中浓硫酸的作用是干燥SO2,所以气流应长进短出,装置为: ,故答案为:
,故答案为: ;
;
(3)装置B内干燥的蓝色石蕊试纸虽然与二氧化硫气体接触,但却不变色,可以说明二氧化硫气体不能使干燥的蓝色石蕊试纸变色;C装置内SO2与水反应生成亚硫酸,酸能使湿润的蓝色石蕊试纸变红,所以实验过程中,说明SO2与水反应生成了酸的实验现象是B中试纸不变色,C中试纸变红色,故答案为:B中试纸不变色,C中试纸变红色;
(4)D装置是尾气处理装置,用氢氧化钠溶液吸收SO2,化学反应方程式为:SO2+2NaOH=Na2SO3+H2O(SO2+NaOH=NaHSO3),故答案为:SO2+2NaOH=Na2SO3+H2O(SO2+NaOH=NaHSO3)。

 名师点拨卷系列答案
名师点拨卷系列答案【题目】如图是元素周期表的一部分,按要求回答问题:
① |
| ||||||||||||||||
|
|
| ② | ③ | ④ |
|
| ||||||||||
⑤ | ⑥ |
|
|
|
|
|
|
|
|
|
| ⑦ |
|
| ⑧ | ⑨ |
|
(1)请写出下列元素的元素符号:①________③_________⑨___________。
(2)元素①④按2:1组成的化合物中化学键为_________。(填“共价键”或“离子键”)
(3)②的单质与⑧的最高价氧化物水化物热的浓溶液反应的化学方程式为____________。
(4)⑤⑥⑦的最高价氧化物水化物的碱性从大到小的顺序____________。(填化学式)
(5)④⑤⑥⑧形成的简单离子,其离子半径由小到大的顺序为____________(填离子符号)。
(6)④和⑧的氢化物稳定性从大到小的顺序为______________________。(填化学式)
(7)元素④的氢化物与⑤发生反应的方程式_____________,所得溶液PH____7(填“>”或“<”或“=”)。
【题目】苯甲醛(微溶于水、易溶于有机溶剂,密度约等于水的密度)在碱性条件下发生歧化反应可以制备苯甲醇(在水中溶解度不大、易溶于有机溶剂,密度约等于水的密度)和苯甲酸。反应原理如下:2C6H5CHO+NaOH→C6H5CH2OH+C6H5COONa、C6H5COONa+HC1→C6H5COOH+NaC1
有关物质物理性质如表:
苯甲醛 | 苯甲醇 | 苯甲酸 | 苯 | |
沸点/℃ | 178 | 205 | 249 | 80 |
熔点/℃ | 26 | -15 | 12 | 5.5 |
苯甲酸在水中的溶解度 | ||
17℃ | 25℃ | 100℃ |
0.21g | 0.34g | 5.9g |
实验流程如图:

(1)第①步需连续加热1小时(如图1),其中加热和固定装置未画出。仪器A的名称为____,若将仪器B改为仪器C,效果不如B,说明原因____。

(2)操作②的实验名称为____。
(3)操作③用沸水浴加热蒸馏,再进行操作④(如图2),收集___℃的馏分。图2中有一处明显错误,正确的应改为____。
(4)抽滤时(如图3)烧杯中苯甲酸晶体转入布氏漏斗时,杯壁上还粘有少量晶体,用___冲洗杯壁上残留的晶体,抽滤完成后用____洗涤晶体。
(5)用电子天平准确称取0.2440g苯甲酸样品于锥形瓶中,加100mL蒸馏水溶解(必要时可以加热),再用0.1000 mol·L-1的标准NaOH溶液滴定,共消耗NaOH溶液19.20mL,滴定选用的指示剂为___,苯甲酸样品的纯度为____%(保留4位有效数字)。
【题目】下列实验中,实验现象及结论都正确且两者具有因果关系的是
实验 | 现象 | 结论 | |
A | 向Ba(NO3)2溶液中通入二氧化硫气体 | 有白色沉淀生成 | SO2与Ba(NO3)2反应得到BaSO3 |
B | 向FeI2的溶液中滴加少量的氯水 | 溶液颜色变深 | Cl2与Fe2+反应生成Fe3+ |
C | 向蔗糖溶液中加几滴稀硫酸,水浴加热5min后,再加新制Cu(OH)2后加热 | 无砖红色沉淀生成 | 蔗糖没有水解 |
D | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
A. A B. B C. C D. D