题目内容
相关数据如下表:
则已知H2(g) + Br2(g) =" 2HBr" (g)△H 为
A.△H =" +" 102kJ/mol B.△H =" -" 102kJ/mol
C.△H =" +" 267kJ/mol D.△H =" -" 267kJ/mol
| | H2(g) | Br2(g) | HBr(g) |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | 200 | 369 |
A.△H =" +" 102kJ/mol B.△H =" -" 102kJ/mol
C.△H =" +" 267kJ/mol D.△H =" -" 267kJ/mol
B
反应热是断键吸收的能量和形成化学键所放出的能量的差值,所以该反应的焓变为△H=436 kJ/mol+200 kJ/mol-2×369 kJ/mol=-102 kJ/mol,所以答案是B。

练习册系列答案
相关题目
 H,其中正确的是( )
H,其中正确的是( )
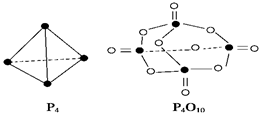
 和
和 。实验测得N-N键键能为167kJ·mol-1,NO2中氮氧双键的平均键能为466 kJ·mol-1,N2O4中氮氧双键的平均键能为438.5 kJ·mol-1。
。实验测得N-N键键能为167kJ·mol-1,NO2中氮氧双键的平均键能为466 kJ·mol-1,N2O4中氮氧双键的平均键能为438.5 kJ·mol-1。 N2O4 (g),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
N2O4 (g),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
 N2O4的平衡常数K将 (填“增大”、“减小”或“不变”)。
N2O4的平衡常数K将 (填“增大”、“减小”或“不变”)。 H1=" +1175.7" kJ·mol-1
H1=" +1175.7" kJ·mol-1