题目内容
某同学做完Zn-Cu-H2SO4组成的原电池的实验后,在读书卡片上作了如下记录,其中合理的是( )

| A、①②③ | B、④⑤⑥ |
| C、③④⑤ | D、②③⑥ |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:铜、锌、稀硫酸构成的原电池中,较活泼的金属作负极,负极上金属失电子发生氧化反应,较不活泼的金属作正极,正极上氢离子得电子发生还原反应,外电路中,电子从负极沿导线流向正极,电解质溶液中阳离子向正极移动,阴离子向负极移动,据此分析解答.
解答:
解:①导线中电流方向:铜→锌,故错误;
②铜极上氢离子得电子生成氢气,所以有气泡生成,故正确;
③锌片失电子生成锌离子进入溶液,导致锌片变薄,故正确;
④反应中失电子的锌作负极,得电子的铜作正极,故错误;
⑤锌比铜活泼,故错误;
⑥原电池放电时,氢离子向铜片移动,硫酸根离子向锌片移动,故正确.
故选D.
②铜极上氢离子得电子生成氢气,所以有气泡生成,故正确;
③锌片失电子生成锌离子进入溶液,导致锌片变薄,故正确;
④反应中失电子的锌作负极,得电子的铜作正极,故错误;
⑤锌比铜活泼,故错误;
⑥原电池放电时,氢离子向铜片移动,硫酸根离子向锌片移动,故正确.
故选D.
点评:本题考查了原电池原理,根据原电池上发生的反应类型、电流的流向等知识来分析解答即可,注意溶液中阴阳离子的移动方向,为易错点.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目
下列说法中正确的是( )
| A、含有金属元素的离子一定是阳离子,金属阳离子被还原一定得到金属单质 |
| B、pH相等的NaOH、NaHCO3和Na2CO3三种溶液:c(NaOH)<c(NaHCO3)<c(Na2CO3) |
| C、常温下,c(NH4+)相等的4种溶液:①(NH4)2SO4 ②(NH4)2Fe(SO4)2 ③NH4Cl ④(NH4)2CO3,溶质物质的量浓度大小关系是:②<①<④<③ |
| D、某温度时水的离子积常数KW=10-13若将此温度下pH=11的NaOH溶液a L与pH=1的稀硫酸b L混合,若所得混合液pH=2,则a:b=2:9 |
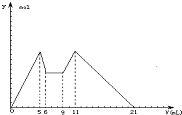 如图是向MgCl2和AlCl3混合液中,先加入NaOH溶液后又滴加盐酸,所得沉淀y(mol)与试剂体积V(mL)之间的关系.以下结论错误的是( )
如图是向MgCl2和AlCl3混合液中,先加入NaOH溶液后又滴加盐酸,所得沉淀y(mol)与试剂体积V(mL)之间的关系.以下结论错误的是( )| A、c(NaOH):c(HCl)=2:1 |
| B、原混合液中c(Al3+):c(Mg2+):c(Cl-)=1:1:5(不考虑离子的水解) |
| C、NaOH和盐酸的分界点是6mL处 |
| D、从7到9,都发生离子反应H++OH-→H2O |
化学与生活密切相关.下列生活中常见物质的俗名与化学式相对应的是( )
| A、苏打-NaHCO3 |
| B、胆矾-CuSO4 |
| C、酒精-CH3OH |
| D、生石灰-CaO |
如图所示,△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,下列说法正确的是( )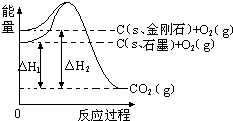

| A、1mol石墨的总键能比1mol金刚石的总键能小1.9kJ |
| B、石墨和金刚石的转化是物理变化 |
| C、金刚石的稳定性强于石墨 |
| D、C(s、石墨)═C(s、金刚石)△H=+1.9kJ?mol-1 |
能在水溶液中大量共存的一组离子是( )
| A、H+、Fe3+、I-、SO42- |
| B、Al3+、Mg2+、HCO3-、Cl- |
| C、K+、Ag+、Ca2+、PO43- |
| D、NH4+、Na+、SO42-、Cl- |
某溶液由Mg2+、Al3+、Cl-、SO42-四种离子组成,测得其中Al3+的物质量浓度为0.3mol/L,SO42-的物质的量浓度为0.4mol/L,Cl-的物质的量浓度为0.3mol/L,则溶液中Mg2+的物质的量浓度为( )
| A、0.2mol/L |
| B、0.1mol/L |
| C、0.05mol/L |
| D、0.4mol/L |