题目内容
19.(1)X、Y形成离子后电子层结构都与氖原子相同,化合物为XY2,X为MgY为F,X与Y间形成离子键.(共价键或离子键)(2)下列各组粒子,属于同种核素的是④(填编号,下同),互为同位素的是③,互为同素异形体的是①,为同一物质的是⑥.
①16O2和18O3
②质子数相同而中子数不同的两种粒子
③${\;}_{1}^{1}$H、D、T
④${\;}_{15}^{30}$R和
 (核内15个中子)
(核内15个中子)⑤葡萄糖和果糖
⑥
 和
和
分析 (1)X、Y形成离子后电子层结构都与氖原子相同,化合物为XY2,则X为Mg、Y为F元素;
(2)质子数相同、中子数相同的原子,属于同种核素;
质子数相同、中子数不同的原子,互为同位素;
由同种元素形成的结构不同的单质互为同素异形体;
分子式相同、结构不同的化合物,互为同分异构体;
分子式相同、结构相同的物质为同一物质.
解答 解:(1)X、Y形成离子后电子层结构都与氖原子相同,化合物为XY2,则X为Mg、Y为F元素,形成的化合物为MgF2,由镁离子与氟离子通过离子键形成,
故答案为:Mg;F;离子;
(2)①16O2和18O3是由元素组成的结构不同的单质,二者核外同素异形体;
②质子数相同而中子数不同的两种粒子,可能互为同位素,也可能是不同的分子或不同分子与离子等,不能确定;
③${\;}_{1}^{1}$H、D、T为H元素的3种同位素;
④${\;}_{15}^{30}$R和 (核内15个中子),均为质子数15、中子数15的P原子,表示同种核素;
(核内15个中子),均为质子数15、中子数15的P原子,表示同种核素;
⑤葡萄糖和果糖 分子式相同,结构不同,互为同分异构体;
⑥ 和
和 分子式相同,且为四面体结构,为同一物质,
分子式相同,且为四面体结构,为同一物质,
故答案为:④;③;①;⑥.
点评 本题考查原子结构与元素性质、化学“五同”概念比较,比较基础,注意对基础知识的理解掌握.

练习册系列答案
相关题目
20.如图为NaCl晶胞,下列说法中正确的是( )
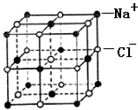

| A. | 每个晶胞中含14个Na+ | |
| B. | Na+的配位数为6,Cl-的配位数也为6 | |
| C. | 与Cl-距离最近的Cl-有12个 | |
| D. | 与Cl-距离最近的Na+形成的几何图形为三角双锥 |
10.下列说法中正确的是( )
| A. | 22.4 L•mol-1就是气体摩尔体积 | |
| B. | 1 mol H2的质量只有在标准状况下才约为2 g | |
| C. | 标准状况下,18 g水的体积为22.4 L | |
| D. | 1 mol H2和O2的混合气体在标准状况下的体积约为22.4 L |
7.已知C(s)+CO2(g)=2CO(g)在常温下为非自发反应(△G>0),下列有关说法正确的是( )
| A. | 该反应是焓减的反应 | |
| B. | 该反应是熵增的反应 | |
| C. | 降低温度可使该反应自发进行 | |
| D. | 无论反应温度是多少,该反应都不能自发进行 |
14.下列说法中正确的是( )
| A. | CO2、NH3、BF3中,所有原子都满足最外层8电子的稳定结构 | |
| B. | 在元素周期表中金属和非金属交界处可以找到半导体材料 | |
| C. | 由非金属元素组成的化合物一定是共价化合物 | |
| D. | 第ⅠA族元素和第ⅦA族元素的原子之间都能形成离子键 |
11.某有机物的结构简式为 ,它的含有醛基(-CHO)的芳香族化合物的同分异构体共有( )
,它的含有醛基(-CHO)的芳香族化合物的同分异构体共有( )
 ,它的含有醛基(-CHO)的芳香族化合物的同分异构体共有( )
,它的含有醛基(-CHO)的芳香族化合物的同分异构体共有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
8.下列有关糖类、油脂、蛋白质的说法正确的是( )
| A. | 蛋白质中只含C、H、O三种元素 | |
| B. | 许多油脂兼有烯烃和酯的性质,可以发生加成反应和水解反应 | |
| C. | 糖类的主要成分是高级脂肪酸甘油酯 | |
| D. | 所有糖、油脂、蛋白质都能发生水解反应 |
9.下列说法正确的是( )
| A. | 活化分子间所发生的碰撞为有效碰撞 | |
| B. | 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使反应速率增大 | |
| C. | 升高温度能增加单位体积内活化分子的百分数和活化分子总数使反应速率增大 | |
| D. | 缩小容器的体积而增大压强,可增加活化分子总数,从而使反应速率增大 |
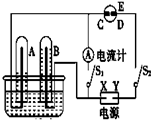 在如图所示的实验装置中,E为一张用淀粉碘化钾溶液润湿的滤纸,C、D为夹在滤纸两端的铂夹,X、Y分别为直流电源的两极.在A、B中充满AgNO3溶液后倒立于盛有AgNO3溶液的水槽中,再分别插入铂电极.切断电源开关S1,闭合开关S2,通直流电一段时间后,B电极质量增重,A极产生无色气体.请回答下列问题:
在如图所示的实验装置中,E为一张用淀粉碘化钾溶液润湿的滤纸,C、D为夹在滤纸两端的铂夹,X、Y分别为直流电源的两极.在A、B中充满AgNO3溶液后倒立于盛有AgNO3溶液的水槽中,再分别插入铂电极.切断电源开关S1,闭合开关S2,通直流电一段时间后,B电极质量增重,A极产生无色气体.请回答下列问题: