题目内容
1.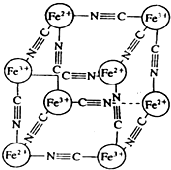 分析化学中常用X射线研究晶体结构,有一种蓝色晶体[可表示为:MxFey(CN)z],研究表明它的结构特性是:Fe2+和Fe3+分别占据立方体的顶点,自身互不相邻,而CN-位于立方体的棱上.其晶体中的阴离子晶胞结构如图示,下列说法不正确的是( )
分析化学中常用X射线研究晶体结构,有一种蓝色晶体[可表示为:MxFey(CN)z],研究表明它的结构特性是:Fe2+和Fe3+分别占据立方体的顶点,自身互不相邻,而CN-位于立方体的棱上.其晶体中的阴离子晶胞结构如图示,下列说法不正确的是( )| A. | 该晶体是离子晶体 | |
| B. | M的离子位于上述晶胞面心,呈+2价 | |
| C. | 晶体的化学式可表示为MFe2(CN)6,且M为+1价 | |
| D. | M的离子位于上述晶胞体心,呈+2价 |
分析 A、该晶体中含有Fe2+、Fe3+、CN-等阴阳离子,据此判断晶体类型;
B、根据晶胞结构,利用均摊法确定晶胞中各离子个数,再根据化合价代数各为零确定M的化合价以及M所处的位置关系;
C、根据晶胞结构,利用均摊法确定晶胞中各离子个数,再根据化合价代数各为零可判断;
D、根据晶胞结构,利用均摊法确定晶胞中各离子个数,再根据化合价代数各为零可判断.
解答 解:A、该晶体中含有Fe2+、Fe3+、CN-等阴阳离子,所以该晶体为离子晶体,故A正确;
B、根据晶胞结构可知,晶胞中含有Fe2+的个数为4×$\frac{1}{8}$=$\frac{1}{2}$,Fe3+的个数为4×$\frac{1}{8}$=$\frac{1}{2}$,CN-的个数为12×$\frac{1}{4}$=3,所以Fe2+、Fe3+、CN-的个数比为1:1:6,根据化合价代数和为零可知,M的化合价为+1价,所以MxFey(CN)z,可表示为MFe2(CN)6,每个晶胞只含有一个M,所以M位于晶胞的体心,故B错误;
C、由B的分析可知,晶体的化学式可表示为MFe2(CN)6,且M为+1价,故C正确;
D、由B的分析可知,M位于晶胞的体心,M为+1价,故D错误;
故选BD.
点评 本题主要考查均摊法计算化学式、晶体结构的确定等知识点,中等难度,有一定的综合性.

练习册系列答案
相关题目
9.下列关于常见有机物的说法不正确的是( )
| A. | 乙烯和苯都能使高锰酸钾溶液褪色 | |
| B. | 乙酸和油脂都能与氢氧化钠溶液反应 | |
| C. | 糖类和蛋白质都是人体重要的营养物质 | |
| D. | 乙烯和甲烷可用溴水鉴别 |
6.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | 使酚酞试液变红的溶液中:S2-、SO42-、SO32-、Na+ | |
| B. | 由水电离出的c(H+)=10-12mol/L的溶液中:Na+、HCO3-、SO42-、K+ | |
| C. | pH=0的溶液中:Na+、K+、Fe2+、NO3- | |
| D. | pH=7的溶液中:Al3+、Cl-、SO42-、CO42- |
10.下列实验操作或原理不正确的是( )
| A. | 纸层析法中的展开剂之所以能够展开的主要原理是毛细现象 | |
| B. | 抽滤时,滤纸要小于布氏漏斗 | |
| C. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| D. | 测定溶液pH的操作:将pH试纸置于表面皿上,用洁净玻璃棒蘸取溶液,点在pH试纸的中部,与对应的标准比色卡比较 |
7.设阿伏加德罗常数的值为NA.下列叙述正确的是( )
| A. | 1.0L 0.1mol/L的NH4Cl溶液中NH4+的个数为0.1NA | |
| B. | 常温下,Cu-Zn原电池中,正极产生1.12LH2时,转移的电子数为0.1NA | |
| C. | 常温下,0.05mol CO2和SO2混合气体中所含氧原子数为0.1NA | |
| D. | 高温高压下,1.4 g N2与0.3 g H2反应,生成的NH3分子数为0.1NA |
 CO2(g)+H2(g)获取。
CO2(g)+H2(g)获取。 mol CO,反应达平衡后,测得CO的浓度为0.08 mol·L-1,则平衡时CO的转化率为 。
mol CO,反应达平衡后,测得CO的浓度为0.08 mol·L-1,则平衡时CO的转化率为 。 位时间内生成amolCO2的同时消耗amolH2
位时间内生成amolCO2的同时消耗amolH2 人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨在燃烧实验中相关的反应有:
人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨在燃烧实验中相关的反应有:

 ⑧
⑧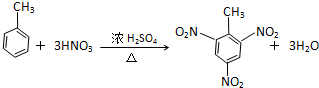 .
.