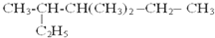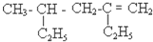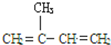题目内容
下面所列问题中,与盐的水解无关的正确说法是( )
①明矾和FeCl3可作净水剂
②实验室保存FeCl3溶液时,要在溶液中加少量盐酸
③在NH4Cl或AlCl3溶液中加入金属镁会产生氢气
④NH4Cl与ZnCl2溶液可作焊接中的除锈剂
⑤实验室盛放Na2CO3、Na2SiO3等溶液的试剂瓶应用橡皮塞,而不能用玻璃塞
⑥长期使用硫铵,土壤酸性增强
⑦NH4Cl和CH3COONH4的浓溶液都可溶解Mg(OH)2沉淀.
①明矾和FeCl3可作净水剂
②实验室保存FeCl3溶液时,要在溶液中加少量盐酸
③在NH4Cl或AlCl3溶液中加入金属镁会产生氢气
④NH4Cl与ZnCl2溶液可作焊接中的除锈剂
⑤实验室盛放Na2CO3、Na2SiO3等溶液的试剂瓶应用橡皮塞,而不能用玻璃塞
⑥长期使用硫铵,土壤酸性增强
⑦NH4Cl和CH3COONH4的浓溶液都可溶解Mg(OH)2沉淀.
| A、④ | B、③⑤ | C、⑦ | D、全有关 |
考点:盐类水解的应用
专题:盐类的水解专题
分析:①明矾和FeCl3都属于含有弱离子的盐,能水解生成胶体;
②氯化铁水解导致溶液呈酸性,加酸抑制水解;
③NH4Cl或AlCl3都水解导致溶液呈酸性,酸和较活泼金属发生置换反应;
④NH4Cl与ZnCl2都水解导致溶液呈酸性,酸和金属氧化物反应生成盐和水;
⑤Na2CO3、Na2SiO3水解导致溶液呈碱性,碱和二氧化硅能反应;
⑥硫酸铵溶液中含有铵根离子,铵根离子水解导致溶液呈酸性;
⑦NH4Cl和CH3COONH4都水解导致溶液呈酸性,酸能和碱反应生成盐和水.
②氯化铁水解导致溶液呈酸性,加酸抑制水解;
③NH4Cl或AlCl3都水解导致溶液呈酸性,酸和较活泼金属发生置换反应;
④NH4Cl与ZnCl2都水解导致溶液呈酸性,酸和金属氧化物反应生成盐和水;
⑤Na2CO3、Na2SiO3水解导致溶液呈碱性,碱和二氧化硅能反应;
⑥硫酸铵溶液中含有铵根离子,铵根离子水解导致溶液呈酸性;
⑦NH4Cl和CH3COONH4都水解导致溶液呈酸性,酸能和碱反应生成盐和水.
解答:
解:①明矾和FeCl3都水解生成胶体,胶体具有吸附性,吸附水中的悬浮物而净水,所以与盐类水解有关,故正确;
②FeCl3为强酸弱碱盐,铁离子水解导致溶液呈酸性,加入酸抑制水解,所以与水解有关,故正确;
③NH4Cl或AlCl3都是强酸弱碱盐,弱离子水解导致溶液呈酸性,酸和金属镁反应生成氢气,与水解有关,故正确;
④NH4Cl与ZnCl2都水解导致溶液呈酸性,酸和金属氧化物反应生成盐和水,所以与水解有关,故正确;
⑤Na2CO3、Na2SiO3都水解导致溶液呈碱性,玻璃中含有二氧化硅,二氧化硅和强碱反应生成粘性的硅酸钠,所以与盐类水解有关,故正确;
⑥硫酸铵是强酸弱碱盐,铵根离子水解导致溶液呈酸性,所以与盐类水解有关,故正确;
⑦NH4Cl和CH3COONH4都水解导致溶液呈酸性,酸和碱反应生成盐和水,与盐类水解有关,故正确;
故选D.
②FeCl3为强酸弱碱盐,铁离子水解导致溶液呈酸性,加入酸抑制水解,所以与水解有关,故正确;
③NH4Cl或AlCl3都是强酸弱碱盐,弱离子水解导致溶液呈酸性,酸和金属镁反应生成氢气,与水解有关,故正确;
④NH4Cl与ZnCl2都水解导致溶液呈酸性,酸和金属氧化物反应生成盐和水,所以与水解有关,故正确;
⑤Na2CO3、Na2SiO3都水解导致溶液呈碱性,玻璃中含有二氧化硅,二氧化硅和强碱反应生成粘性的硅酸钠,所以与盐类水解有关,故正确;
⑥硫酸铵是强酸弱碱盐,铵根离子水解导致溶液呈酸性,所以与盐类水解有关,故正确;
⑦NH4Cl和CH3COONH4都水解导致溶液呈酸性,酸和碱反应生成盐和水,与盐类水解有关,故正确;
故选D.
点评:本题考查了盐类水解,明确“谁强谁显性、谁弱谁水解”等知识点来分析解答即可,题目难度不大.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案
相关题目
下列常见有机物中,既能发生取代反应,又能使溴的CCl4溶液反应褪色的是( )
| A、甲苯 |
B、 |
| C、植物油 |
| D、CH3COOH |
1000C时,将0.40mol二氧化氮气体充入2L密闭容器中,发生反应2NO2(g)?N2O4(g)△H=-57kJ?mol-1,每隔一段时间对该容器内的物质进行分析.得到数据如下表所示:
下列说法正确的是( )
| 时间/s | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
| A、反应开始20s内,用二氧化氮表示的平均反应速率为0.005mol?L-1?s-1 |
| B、保持其他条件不变,若起始时向容器中充入0.30mol NO2和0.10mol N2O4,则此时v正<v逆 |
| C、80s时向容器中再加入0.32mol氮气,同时将容器扩大为4L,则平衡不移动 |
| D、保持其他条件不变,向容器中再充入是0.20mol NO2,达到平衡时,NO2的体积分数减小 |
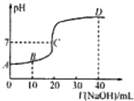 25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL 0.1000mol/L的CH3COOH.滴定曲线如图所示.下列分析错误的是( )
25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL 0.1000mol/L的CH3COOH.滴定曲线如图所示.下列分析错误的是( )| A、C点的溶液:c(CH3COO-)+c(CH3COOH)>c(Na-) |
| B、B点的溶液:c(CH3COO-)>(Na+)>c(H-)>c(OH-) |
| C、A点的纵坐标值为1 |
| D、D点溶液2c(CH3COOH)+c(H+)=c(OH-)-c(CH3COO-) |
V L含有(NH4)2SO4、NH4NO3的混合溶液,加入a mol NaOH后加热,恰好使NH3全部逸出;又加入b mol BaCl2,刚好使SO42-完全沉淀.则原混合溶液中NH4NO3的物质的量浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列比较正确的是( )
| A、电负性:As>S>P |
| B、第一电离能F>N>O |
| C、熔点.BN>CCl4>MgBr2 |
| D、溶解性:乙醛>苯酚>乙醇 |