题目内容
11.下列实验操作或结论正确的是( )| A. | 在某溶液中加入AgN03溶液有白色沉淀产生,再加盐酸,沉淀不消失,则该溶液中一定有CI- | |
| B. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有C032- | |
| C. | 做焰色反应前应先将铂丝在稀硫酸中洗干净再蘸取待测液进行实验 | |
| D. | 如透过蓝色的钴玻璃能够观察到紫色火焰,则肯定有K元素,可能有Na元素 |
分析 A.能和银离子反应生成白色沉淀的阴离子有碳酸根离子、氯离子等;
B.能使澄清石灰水变浑浊的气体有二氧化碳和二氧化硫;
C.作焰色反应前应先将铂丝在稀盐酸中洗干净再蘸取待测液进行实验;
D.蓝色钴玻璃可滤去黄光.
解答 解:A.在某溶液中加入AgNO3溶液有白色沉淀产生,该白色沉淀可能是碳酸银,碳酸银和盐酸反应转化为氯化银白色沉淀,所以原溶液中不一定含有氯离子,故A错误;
B.能使澄清石灰水变浑浊的气体有二氧化碳和二氧化硫,能和稀盐酸反应生成二氧化碳气体的物质中可能含有碳酸根离子,也可能含有碳酸氢根离子,故B错误;
C.为除去实验物质用盐酸洗涤,再灼烧至跟酒精灯火焰颜色相同后再使用,盐酸可以溶解氧化物等杂质 且易挥发不会残留痕迹,所以选用盐酸洗涤而不是硫酸洗涤,故C错误;
D.蓝色钴玻璃可滤去黄光,不能确定是否含有钠离子,故D正确;
故选D.
点评 本题考查化学实验方案的评价,侧重于离子的检验的考查,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质以及实验的严密性的评价,难度不大.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
1.下列各组离子在无色碱性溶液中能大量共存的是( )
| A. | Na+、H+、MnO4-、SO42- | B. | Na+、K+、NO3-、SO42- | ||
| C. | Fe2+、Cl-、CO32-、SiO32- | D. | Mg2+、Na+、Cl-、HCO3- |
6.下列关于仪器的识别中错误的是( )
| A. | 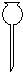 分液漏斗 | B. |  蒸发皿 | C. | 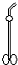 坩埚钳 | D. |  滴瓶 |
16.体积均为100mL,浓度均为1mol.L-1的盐酸和硫酸溶液,分别加入质量相等的镁块充分反应,所生成的气体在相同条件下体积比为2:3,则镁块的质量为( )
| A. | 1.8 g | B. | 2.4g | C. | 3.6g | D. | 4.8g |
3.下列说法正确的是( )
| A. | 电解质的水溶液一定能导电 | |
| B. | 非电解质的水溶液一定不能导电 | |
| C. | 酸、碱和盐类都属于电解质,其他化合物都是非电解质 | |
| D. | 电解质是在水溶液里或熔融状态下因本身能电离出阳离子和阴离子而导电的化合物 |
20.在一定温度下,可逆反应X(g)+3Y(g)?2Z(g)达到平衡的标志是( )
| A. | 单位时间生成a mol X,同时生成3 a mol Y | |
| B. | Z的生成速率与Z的分解速率相等 | |
| C. | X、Y、Z的浓度相等 | |
| D. | X、Y、Z的分子个数比为1:3:2 |
1.以下有关原子结构及元素周期律的叙述正确的是( )
| A. | 同周期元素(除0族元素外)从左到右,原子半径逐渐减小 | |
| B. | 第IA族元素铯的两种同位素137Cs比133Cs多4个质子 | |
| C. | 第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强 | |
| D. | 若M+和R2-的核外电子层结构相同,则原子序数:R>M |