题目内容
1.以下有关原子结构及元素周期律的叙述正确的是( )| A. | 同周期元素(除0族元素外)从左到右,原子半径逐渐减小 | |
| B. | 第IA族元素铯的两种同位素137Cs比133Cs多4个质子 | |
| C. | 第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强 | |
| D. | 若M+和R2-的核外电子层结构相同,则原子序数:R>M |
分析 A.同周期,原子半径随原子序数增大而减小;
B.同位素的质子数相同;
C.第ⅦA族元素从上到下,元素的非金属性减弱;
D.M+和R2-的核外电子层结构相同,则M在R的下一周期.
解答 解:A.同周期,原子半径随原子序数增大而减小,则同周期元素(除0族元素外)从左到右,原子半径逐渐减小,故A正确;
B.同位素的质子数相同,则第IA族元素铯的两种同位素137Cs、133Cs的质子数相同,故B错误;
C.第ⅦA族元素从上到下,元素的非金属性减弱,则从上到下,其氢化物的稳定性逐渐减弱,故C错误;
D.M+和R2-的核外电子层结构相同,则M在R的下一周期,可知原子序数:R<M,故D错误;
故选A.
点评 本题考查元素周期表的结构及应用,为高频考点,把握元素的位置与性质、元素周期律为解答该题的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
11.下列实验操作或结论正确的是( )
| A. | 在某溶液中加入AgN03溶液有白色沉淀产生,再加盐酸,沉淀不消失,则该溶液中一定有CI- | |
| B. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有C032- | |
| C. | 做焰色反应前应先将铂丝在稀硫酸中洗干净再蘸取待测液进行实验 | |
| D. | 如透过蓝色的钴玻璃能够观察到紫色火焰,则肯定有K元素,可能有Na元素 |
12.设NA为阿伏伽德罗常数的数值,下列说法中正确的是( )
| A. | 46 g乙醇中含有的化学键数为7NA | |
| B. | 1 mol OH-和1 mol-OH含有的电子数均为10NA | |
| C. | 标准状况下,6.72 L NO2和水充分反应转移电子数为0.2NA | |
| D. | 常温常压下,28 g 乙烯分子中共含有2NA对共用电子对 |
9.将40mL0.5mol/L Na2CO3溶液加水稀释到500mL,稀释后溶液中Na2CO3的物质的量浓度为( )
| A. | 0.03mol/L | B. | 0.3mol/L | C. | 0.04mol/L | D. | 0.4mol/L |
7.实验室常用NaNO2和NH4Cl反应制取N2:NaNO2+NH4Cl═NaC1+N2↑+2H2O.下列说法正确的是( )
| A. | NaNO2是还原剂 | |
| B. | NH4Cl中N元素被还原 | |
| C. | 生成1molN2时转移6mol电子 | |
| D. | 氧化剂和还原剂的物质的量之比是1:1 |
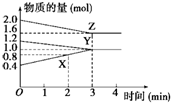 (1)某温度时,在3L密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示,由图中数据分析:
(1)某温度时,在3L密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示,由图中数据分析: