题目内容
【题目】已知煤的近代结构模型如图所示。
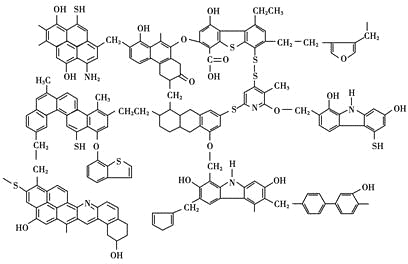
回答下列问题:
(1)从煤的结构模型来看,煤是工业上获得____________的重要来源。
(2)我国大约70%的煤是直接用于燃烧的。从煤的结构模型来看,在提供热量的同时产生大量的____________、____________等气体物质,造成严重的大气污染。
(3)“型煤”技术不仅可以减少87%的废气排放量,烟尘排放量也可减少80%,致癌物苯并[α]芘的排放量也减少,同时节煤20%~30%。“型煤”技术的原理是利用固硫剂在燃烧过程中生成稳定的硫酸盐。某“型煤”生产厂利用石灰石作固硫剂,试用化学方程式表示其固硫过程________________、________________。
(4)为了解决煤燃烧所造成的污染问题和提高煤的利用价值,煤资源的综合利用方法还有____________、____________、____________等。
【答案】芳香烃 SO2 氮氧化物 CaCO3![]() CaO+CO2↑ 2CaO+2SO2+O2
CaO+CO2↑ 2CaO+2SO2+O2![]() 2CaSO4 干馏 气化 液化
2CaSO4 干馏 气化 液化
【解析】
(1)从煤的结构模型图可以看出,它是工业上获得芳香烃的重要来源。
(2)煤中含C、H、O、S、N元素,煤直接燃烧在提供热量的同时会产生SO2、氮氧化物而污染大气。
(3)石灰石固硫实际上是利用CaCO3分解产生的CaO结合SO2,在煤燃烧时生成CaSO4,此过程中反应的化学方程式为CaCO3![]() CaO+CO2↑、2CaO+2SO2+O2
CaO+CO2↑、2CaO+2SO2+O2![]() 2CaSO4。
2CaSO4。
(4)煤资源的综合利用方法还有:煤的干馏、煤的气化、煤的液化等。

【题目】为确定某NH4NO3和(NH4)2SO4混合物的组成,称取4份样品分别加入50.0mL相同浓度的NaOH溶液中,加热充分反应(加热后氨气全部逸出)。加入的混合物的质量和产生的气体体积(标准状况)的关系如下表:
实验序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
NaOH溶液体积(mL) | 50.0 | 50.0 | 50.0 | 50.0 |
样品质量(g) | 3.44 | m | 17.2 | 21.5 |
NH3体积(L) | 1.12 | 2.24 | 5.60 | 5.60 |
试计算:
(1)m=________g;c(NaOH)=___________ mol·L-1
(2)样品中NH4NO3和(NH4)2SO4物质的量之比为______________。