题目内容
【题目】![]() 都是非极性分子,
都是非极性分子,![]() 都是极性分子,由此推测ABn型分子是非极性分子的经验规律是( )
都是极性分子,由此推测ABn型分子是非极性分子的经验规律是( )
A.所有原子在同一平面上B.分子中每个键的键长应相等
C.A的相对原子质量小于BD.在ABn中A原子没有孤电子对
【答案】D
【解析】
共价键的极性是由于成键两原子对电子的引力不同,而使共用电子对不在中央,发生偏移,导致键两端显部分的电性之故,ABn型分子中A原子的所有价电子都参与成键,与相对原子质量大小及健长无关。
A.分子中所有原子不一定都在同一平面上,如CH4是正四面体结构,故A错误;
B.H2O分子中两个OH键的键长都相等,但水分子是极性分子,故B错误;
C.PCl3分子中P原子量小于Cl原子,但PCl3是极性分子,故C错误;
D.在ABn分子中A原子的所有价电子都构成共价键,没有孤电子对,导致结构对称、正负电荷重心重叠,所以为非极性分子,故D正确;
故答案选D。

 阅读快车系列答案
阅读快车系列答案【题目】现有部分前36号元素的性质或原子结构信息如下表:
元素编号 | 元素的性质或原子结构 |
R | 基态原子的最外层有3个未成对电子,次外层有2个电子 |
S | 单质能与水剧烈反应,所得溶液a弱酸性 |
T | 基态原子3d轨道上有1个电子 |
X |
|
(1)R元素的第一电离能要大于其同周期相邻的元素,原因是______。
(2)S元素的常见化合价为_______,原因是_______。
(3)T元素的原子N电子层上的电子数为____________。
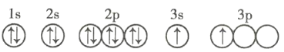
(4)X的轨道表示式违背了____________。用X单质、碱金属盐等可以制作焰火。燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:___________。
【题目】根据杂化轨道理论和价电子对互斥理论模型判断,下列分子或离子的中心原子杂化方式及空间构型正确的是( )
选项 | 分子或离子 | 中心原子杂化方式 | 价电子对互斥理论模型 | 分子或离子的空间构型 |
A | H2O | sp1 | 直线形 | 直线形 |
B | BBr3 | sp2 | 平面三角形 | 三角锥形 |
C | PCl3 | sp2 | 四面体形 | 平面三角形 |
D | CO32- | sp2 | 平面三角形 | 平面三角形 |
A.AB.BC.CD.D