题目内容
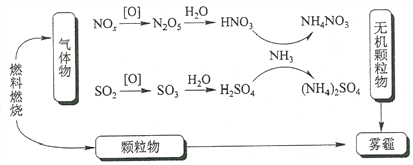
【题目】已知某些元素在周期表中的位置如图所示:

下列说法正确的是( )
A.表中五种元素位于5个不同的区
B.元素4的基态原子的价电子排布式为3d104s2与它具有相同最外层电子数的元素只可能处于ds区
C.元素1、2、3的基态原子中,未成对电子数之比为1:3:5
D.元素5的原子结构示意图为:
【答案】D
【解析】
根据周期表中的位置,可判断1为H;2为O;3为Mn;4为Zn;5为Ge。
A.H在s区;O、Ge在p区;Mn在d区;Zn在ds区,表中五种元素位于4个不同的区,A说法错误;
B.元素4为Zn,其基态原子的价电子排布式为3d104s2,最外层电子排布为4s2,与它具有相同最外层电子数的元素可能处于ds区或s区,B说法错误;
C.元素1、2、3的基态原子中,未成对电子数分别为1、2、5,比值为1:2:5,C说法错误;
D.元素5为Ge,核外电子排布式为1s22s22p63s23p63d104s24p2,则原子结构示意图为: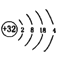 ,D说法正确;
,D说法正确;
答案为D。

练习册系列答案
相关题目