题目内容
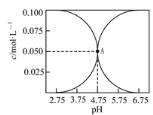
【题目】常温下,有c(CH3COOH)+c(CH3COO-)=0.1 mol·L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH的关系如下图所示。下列溶液中离子浓度关系正确的是
A.c(Na+)=0.1 mol·L-1的溶液中: c(H+)+c(CH3COOH)=c(OH-)
B.点A溶液中:c(Na+)>c(CH3COOH)
C.pH=3.5的溶液中:c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
D.c(CH3COO-)=0.025 mol·L-1的溶液中:3c(Na+)<c(CH3COOH)
【答案】AD
【解析】
结合物质性质观察图可知,随着pH值的增大,浓度降低的是CH3COOH,浓度升高的是CH3COO-,在pH=4.75时,c(CH3COOH) =c(CH3COO-),可在此认识基础上对各选项作出判断。
A. 根据电荷守恒有:c(H+)+c(Na+)=c(OH-)+c(CH3COO-),根据物料守恒有:c(CH3COO-)+c(CH3COOH)=c(Na+),将两等式相加得: c(H+)+c(CH3COOH)=c(OH-),A选项正确;
B. 根据电荷守恒有:c(H+)+c(Na+)=c(OH-)+c(CH3COO-),点A溶液pH=4.75,显酸性,c(H+)>c(OH-),所以,c(Na+)<c(CH3COOH),B选项错误;
C. pH=3.5时,溶液显酸性,c(H+)>c(OH-),所以,c(Na+)<c(CH3COOH),C选项错误;
D. 根据电荷守恒有:c(H+)+c(Na+)=c(OH-)+c(CH3COO-),c(CH3COO-)=0.025 mol·L-1的溶液显酸性,c(H+)>c(OH-),所以, c(Na+)=c(OH-)-c(H+)+c(CH3COO-)<c(CH3COO-)=![]() c(CH3COOH),即,3c(Na+)<c(CH3COOH),D选项正确;
c(CH3COOH),即,3c(Na+)<c(CH3COOH),D选项正确;
答案选AD。

 53随堂测系列答案
53随堂测系列答案【题目】对分别盛有不同无色溶液的①②③④四支试管进行如下操作。现象和结论对应正确的是( )
选项 | 操作 | 现象 | 结论 |
A | 向①中滴加 | 试纸变蓝 | 原溶液中有 |
B | 向②中滴入 | 有白色沉淀生成 | 原溶液中有 |
C | 向③中先滴加 | 生成白色沉淀 | 原溶液中有 |
D | 向④中滴加氯水和 | 下层溶液呈橙色 | 原溶液中有 |
A.AB.BC.CD.D