题目内容
将2 mol SO2和2 mol SO3气体混合于某固定体积的密闭容器中,在一定条件下反应:
2SO2+O2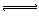 2SO3(气)
2SO3(气)
平衡时SO3为W mol。相同温度下,分别按下列配比在相同体积的容器中反应,反应达到平衡时,SO3物质的量大于W mol的是
A.2molSO2+1molO2
B.4 mol SO2+1 mol O2</PGN0033B.TXT/PGN>
C.2 mol SO2+1 mol O2+2 mol SO3
D.3 mol SO2+1 mol SO3
2SO2+O2
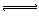 2SO3(气)
2SO3(气)平衡时SO3为W mol。相同温度下,分别按下列配比在相同体积的容器中反应,反应达到平衡时,SO3物质的量大于W mol的是
A.2molSO2+1molO2
B.4 mol SO2+1 mol O2</PGN0033B.TXT/PGN>
C.2 mol SO2+1 mol O2+2 mol SO3
D.3 mol SO2+1 mol SO3
C、D
利用极端假设法分析,2 molSO3完全转化成反应物时,可生成 1molO2和2 molSO2。则起始原料2mol SO2和 2 molSO3和4 molSO2+1molO2相当。该配比量与所选答案相比A小于,B相等,C,D配比量均相当于4 molSO2+2 molO2,大于起始配比量,所以SO3的物质的量大于W mol的是C,D,小于W mol的是A。

练习册系列答案
相关题目
 2HI(g),通入xmol H2和ymol I2 蒸气,在下列条件下发生反应达到平衡,改变下列条件,正、逆反应速率会发生什么变化(增加、减小、不变)?分别填在横线上。
2HI(g),通入xmol H2和ymol I2 蒸气,在下列条件下发生反应达到平衡,改变下列条件,正、逆反应速率会发生什么变化(增加、减小、不变)?分别填在横线上。 (5).增大容器的体积, v正 v逆
(5).增大容器的体积, v正 v逆  3C(g)+2D(g) ΔH<0,后甲容器内的反应达到化学平衡,A的浓度为2.4mol·L-1,B的浓度为1.8mol·L-1;tmin后乙容器达到化学平衡,B的浓度为0.8mol·L-1。根据题目给的信息回答下列问题:
3C(g)+2D(g) ΔH<0,后甲容器内的反应达到化学平衡,A的浓度为2.4mol·L-1,B的浓度为1.8mol·L-1;tmin后乙容器达到化学平衡,B的浓度为0.8mol·L-1。根据题目给的信息回答下列问题: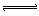 cC(气)+dD(气)+Q如果升高温度或降低压强,则C(气)的物质的量都增大,试判断下列各组关系,哪组是正确的
cC(气)+dD(气)+Q如果升高温度或降低压强,则C(气)的物质的量都增大,试判断下列各组关系,哪组是正确的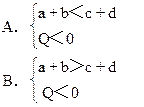
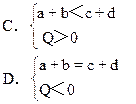
 pC(气)+qD(气)+ Q有下列判断,其中正确的是
pC(气)+qD(气)+ Q有下列判断,其中正确的是 