题目内容
【题目】第三代太阳能电池就是铜铟镓硒CIGS等化合物薄膜太阳能电池以及薄膜Si系太阳能电池。
(1)晶体硅中Si原子的杂化方式是___,基态Ga原子核外电子排布式为___。
(2)向硫酸铜溶液中逐滴滴加浓氨水,先出现蓝色絮状沉淀,后沉淀逐渐溶解得到[Cu(NH3)4]SO4的深蓝色透明溶液。
①NH3极易溶于水,除因为NH3与H2O都是极性分子外,还因为____。
②在[Cu(NH3)4]2+中Cu2+与NH3之间形成的化学键称为___,提供孤电子对的成键原子是___。
③[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个C1-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为___。
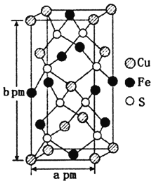
(3)某含铜化合物的晶胞如图所示,晶胞上下底面为正方形,侧面与底面垂直。则晶胞中每个Cu原子与____个S原子相连,含铜化合物的化学式为____。设NA为阿伏加德罗常数的值,则该晶胞的密度为___gcm3(用含a、b、NA的代数式表示)。
【答案】sp3 1s22s22p63s23p63d104s24p1或[Ar]3d104s24p1 NH3与H2O之间可形成分子间氢键,NH3与H2O发生反应 配位键 N 平面正方形 4 CuFeS2 ![]()
【解析】
(1)根据晶体硅中每个Si原子与周围的4个硅原子形成正四面体,向空间延伸的立体网状结构判断;Ga是31号元素,根据能量最低原理书写核外电子排布式;
(2)①氨气分子与水分子之间形成氢键,且氨气能与水反应;
②Cu2+含有空轨道,NH3中N原子含有孤电子对;
③[Cu(NH3)4]2+中的两个NH3被两个Cl-取代能得到两种不同结构的产物,[Cu(NH3)4]2+的空间构型为平面正方形;
(3)根据均摊法计算晶胞中各原子数目,确定化学式,进而计算晶胞质量,再根据![]() 计算晶胞密度。
计算晶胞密度。
(1)因晶体硅中每个Si原子与周围的4个硅原子形成正四面体,向空间延伸的立体网状结构,所以晶体硅中Si原子的杂化方式为sp3杂化。Ga位于周期表中第4周期第ⅢA族,则基态Ga原子的核外电子排布式为1s22s22p63s23p63d104s24p1或[Ar]3d104s24p1,故答案为:sp3;1s22s22p63s23p63d104s24p1或[Ar]3d104s24p1;
(2)①NH3极易溶于水,除因为它们都是极性分子外,还因为:NH3与H2O之间可形成分子间氢键,NH3与H2O发生反应,故答案为:NH3与H2O之间可形成分子间氢键,NH3与H2O发生反应;
②Cu2+含有空轨道,NH3中N原子含有孤电子对,二者形成配位键,故答案为:配位键;N;
③[Cu(NH3)4]2+中的两个NH3被两个Cl-取代能得到两种不同结构的产物,[Cu(NH3)4]2+的空间构型为平面正方形,故答案为:平面正方形;
(3)晶胞中D(S)原子位于晶胞内部,原子数目为8个,E(Fe)原子6个位于面上、4个位于棱上,E(Fe)原子数目=6×![]() +4×
+4×![]() =4,F(Cu)原子位于4个位于面上、1个内部、8个顶点上,原子数目=4×
=4,F(Cu)原子位于4个位于面上、1个内部、8个顶点上,原子数目=4×![]() +1+8×
+1+8×![]() =4,晶体中Cu、Fe、S原子数目之比=4:4:8=1:1:2,故该晶体化学式为:CuFeS2,
=4,晶体中Cu、Fe、S原子数目之比=4:4:8=1:1:2,故该晶体化学式为:CuFeS2,
晶胞质量m=![]() ×4g,晶胞体积V=(a×10-10cm)2×b×10-10cm,
×4g,晶胞体积V=(a×10-10cm)2×b×10-10cm,
晶体密度ρ=(![]() ×4g)÷[(a×10-10cm)2×b×10-10cm]=
×4g)÷[(a×10-10cm)2×b×10-10cm]=![]() gcm3,
gcm3,
故答案为:4;CuFeS2;![]() 。
。

【题目】下列有关反应热的叙述中正确的是 ( )
①已知2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ· mol-1,则氢气的燃烧热ΔH=-241.8 kJ· mol-1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g)![]() Z(g)+W(s) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大
Z(g)+W(s) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大
④已知:下表数据可以计算出![]() (g)+3H2(g)
(g)+3H2(g)![]()
![]() (g)的焓变
(g)的焓变
共价键 | C—C | C=C | C—H | H—H |
键能/(kJ·mol-1) | 348 | 610 | 413 | 436 |
⑤根据盖斯定律可推知在相同条件下,金刚石或石墨燃烧生成1 mol CO2(g)时,放出的热量相等
⑥25 ℃、101 kPa时,1 mol碳完全燃烧生成CO2(g)所放出的热量为碳的燃烧热
A.①②③④B.③④⑤C.④⑤D.⑥