题目内容
13.下列化学用语不正确的是( )| A. | 铀(U)的两种核素:${\;}_{92}^{235}$U和${\;}_{92}^{238}$U | |
| B. | CO2的结构式:O=C=O | |
| C. | 乙醇分子的比例模型: | |
| D. | Cl-结构示意图: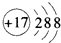 |
分析 A、质子数相同,中子数不同的同种元素的不同种元素互为同位素,每种原子均是一种核素;
B、二氧化碳为直线形分子,C分别与O形成2对共价键;
C、比例模型主要体现出原子的相对体积大小,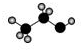 为乙醇的球棍模型;
为乙醇的球棍模型;
D、Cl为17号元素,得到1个电子后最外层电子数满足8个电子的稳定结构,为氯离子.
解答 解:A、${\;}_{92}^{235}$U和${\;}_{92}^{238}$U是U元素的两种不同的核素,故A正确;
B、二氧化碳为直线形分子,结构式为O=C=O,故B正确;
C、乙醇的比例模型中,应该体现出各原子的相对体积大小,乙醇正确的比例模型为: ,故C错误;
,故C错误;
D、Cl为17号元素,得到1个电子后最外层电子数满足8个电子的稳定结构,变为带1个负电荷的氯离子,结构示意图为: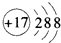 ,故D正确,故选C.
,故D正确,故选C.
点评 本题主要考查的是常见化学用语,涉及离子结构示意图、结构式、比例模型与球棍模型的比较等,难度不大.

练习册系列答案
相关题目
4.下列物质中属于弱电解质的是( )
| A. | 氨水 | B. | 金属铜 | C. | 醋酸 | D. | 苯 |
1.下列事实不能用化学平衡移动原理解释的是( )
| A. | 收集氯气可以用排饱和食盐水的方法 | |
| B. | 可用浓氨水和氢氧化钠固体快速制取氨气 | |
| C. | 加催化剂,使N2和H2在一定的条件下转化为NH3 | |
| D. | 20℃时,AgCl在蒸馏水中的溶解度比在0.1mol/LNaCl溶液中的溶解度大 |
18.部分短周期元素的原子结构及相关性质如表所示:
请回答:
(1)T在元素周期表中的位置为第三周期第ⅥA族.
(2)X的一种同位素可用于测定文物年代,该同位素为614C(用原子符号表示).
(3)Z单质的电子式为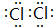 ;Y的氢化物的水溶液显碱性的原因为NH3+H2O?NH3•H2O?NH4++OH-(用离子方程式表示).
;Y的氢化物的水溶液显碱性的原因为NH3+H2O?NH3•H2O?NH4++OH-(用离子方程式表示).
(4)Z与T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是d(填选项字母)
a.常温下,Z单质为气体,T单质为固体
b.Z的氢化物的水溶液的酸性比T强
c.Z的最高正价比Y高
d.最高价氧化物对应水化物的酸性Z比T强
(5)Z的氢化物与Y的氢化物发生化合反应,产物中含有的化学键类型为离子键、共价键.
| 元素编号 | 元素性质或原子结构 |
| T | 最高正价与最低负价的代数和为4 |
| X | 最外层电子数是次电子数次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
| Z | 最高正价是+7价 |
(1)T在元素周期表中的位置为第三周期第ⅥA族.
(2)X的一种同位素可用于测定文物年代,该同位素为614C(用原子符号表示).
(3)Z单质的电子式为
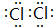 ;Y的氢化物的水溶液显碱性的原因为NH3+H2O?NH3•H2O?NH4++OH-(用离子方程式表示).
;Y的氢化物的水溶液显碱性的原因为NH3+H2O?NH3•H2O?NH4++OH-(用离子方程式表示).(4)Z与T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是d(填选项字母)
a.常温下,Z单质为气体,T单质为固体
b.Z的氢化物的水溶液的酸性比T强
c.Z的最高正价比Y高
d.最高价氧化物对应水化物的酸性Z比T强
(5)Z的氢化物与Y的氢化物发生化合反应,产物中含有的化学键类型为离子键、共价键.
5.a、b、c、d是四种短周期元素,a、b、d同周期,c、d同主族,a的原子结构示意图为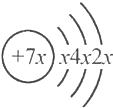 ,b与c形成的化合物的化学式为b3c,且b、c离子有相同的电子层结构,下列比较中,正确的是( )
,b与c形成的化合物的化学式为b3c,且b、c离子有相同的电子层结构,下列比较中,正确的是( )
 ,b与c形成的化合物的化学式为b3c,且b、c离子有相同的电子层结构,下列比较中,正确的是( )
,b与c形成的化合物的化学式为b3c,且b、c离子有相同的电子层结构,下列比较中,正确的是( )| A. | 原子序数:a>b>c | B. | 氢化物的稳定性:a>c>d | ||
| C. | 原子半径:d>a>c | D. | 最高价含氧酸的酸性:d>c>a |
2.在下列各溶液中,离子一定能大量共存的是( )
| A. | 强碱性溶液中:K+、Al3+、Cl-、SO42- | |
| B. | 含有0.1 mol/L Fe3+的溶液中:K+、Mg2+、I-、Cl- | |
| C. | 含有0.1 mol/L Ca2+的溶液中:Na+、K+、SO42-、Cl- | |
| D. | 室温下,pH=1的溶液中:Na+、Fe3+、NO-3、SO42- |