题目内容
6.离子方程式2Ca2++3HCO3-+3OH-═2CaCO3↓+CO32-+3H2O可以表示( )①Ca(HCO3)2与NaOH溶液反应
②NaHCO3与澄清石灰水反应
③Ca(HCO3)2与澄清石灰水反应
④NH4HCO3与澄清石灰水反应.
| A. | ①②③④ | B. | ①②③ | C. | ①②④ | D. | ①② |
分析 ①2mol碳酸氢钙与3mol氢氧化钠反应生成碳酸钙、碳酸钠、碳酸氢钠和水;
②碳酸氢钠与氢氧化钙按照物质的量之比3:2反应生成碳酸钙、碳酸钠和碳酸氢钠、水;
③Ca(OH)2与Ca(HCO3)2反应生成碳酸钙和水;
④NH4HCO3与足量澄清石灰水的反应生成碳酸钙、一水合氨和水,NH4HCO3与少量澄清石灰水反应生成碳酸钙、碳酸铵和水.
解答 解:①2mol碳酸氢钙与3mol氢氧化钠反应生成碳酸钙、碳酸钠、碳酸氢钠和水,离子方程式:2Ca2++3HCO3-+3OH-═2CaCO3↓+CO32-+3H2O,故选;
②碳酸氢钠与氢氧化钙按照物质的量之比3:2反应生成碳酸钙、碳酸钠和碳酸氢钠、水,离子方程式:2Ca2++3HCO3-+3OH-═2CaCO3↓+CO32-+3H2O,故选;
③Ca(OH)2与少量的Ca(HCO3)2反应的离子反应为Ca2++HCO3-+OH-=CaCO3↓+H2O,Ca(OH)2与足量的Ca(HCO3)2反应的离子反应为Ca2++HCO3-+OH-=CaCO3↓+H2O,故不选;
④NH4HCO3与足量澄清石灰水的离子反应为NH4++Ca2++HCO3-+2OH-=CaCO3↓+NH3.H2O+H2O,NH4HCO3与少量澄清石灰水的离子反应为Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O,故不选;
故选:D.
点评 本题考查了离子方程式的书写,侧重考查反应物用量对反应的影响,明确反应实质是解题关键,题目难度中等.

练习册系列答案
相关题目
11.下列离子方程式正确的是( )
| A. | 向漂白粉溶液中通入少量二氧化硫:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| B. | 稀硝酸中加入过量铁粉:Fe+4H++NO-3═Fe3++NO↑+2H2O | |
| C. | 溴化亚铁溶液中通入足量氯气:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | 苯酚钠溶液中通入少量二氧化碳: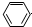 -O-+CO2+H2O→ -O-+CO2+H2O→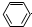 -OH+HCO3- -OH+HCO3- |
17.一定温度下,在一固定体积的密闭容器中,可逆反应A(s)+3B(g)?2C(g)达到平衡时,下列说法正确的是( )
①C的生成速率和C的分解速率相等 ②单位时间内生成a mol A,同时生成3a mol B
③气体密度不再变化 ④混合气体的总压强不再变化 ⑤A、B、C的物质的量之比为1:3:2
⑥混合气体的平均相对分子质量不变.
①C的生成速率和C的分解速率相等 ②单位时间内生成a mol A,同时生成3a mol B
③气体密度不再变化 ④混合气体的总压强不再变化 ⑤A、B、C的物质的量之比为1:3:2
⑥混合气体的平均相对分子质量不变.
| A. | ②④⑤ | B. | ①③④⑥ | C. | ①②④⑥ | D. | ①②③④⑤ |
14.100℃时pH=3的盐酸和pH=9的氢氧化钠溶液以体积比11:9混合,混合液的pH为( )
| A. | 约3.3 | B. | 8 | C. | 6 | D. | 4 |
16.有一粗硅,含杂质铁,取等质量的样品分别投入足量的稀盐酸和足量的稀氢氧化钠溶液中,放出等量的H2,则该粗硅中铁和硅的关系正确的是( )
| A. | 物质的量之比为1:1 | B. | 物质的量之比为1:2 | ||
| C. | 质量之比为4:1 | D. | 质量之比为2:1 |
 Al(OH)3+OH-.
Al(OH)3+OH-.
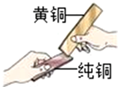 合金是重要的金属材料.
合金是重要的金属材料.