题目内容
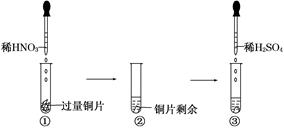
某实验过程如图所示,则图③试管中的现象是

| A.铜片溶解,产生无色气体,该气体遇空气变为红棕色 |
| B.铜片溶解,产生无色气体,该气体遇到空气不变色 |
| C.铜片溶解,放出红棕色有刺激性气味的气体 |
| D.无明显现象,因稀硫酸不与铜反应 |
A
试题分析:在②试管的溶液中仍然有NO3-,加入稀硫酸,相当于有硝酸存在,所以铜片溶解、产生无色气体NO,该气体遇空气变为红棕色。A项正确。

练习册系列答案
相关题目
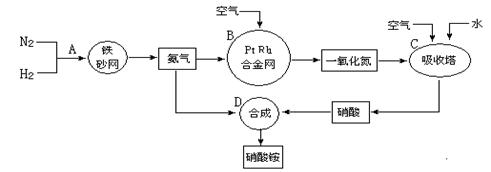

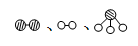 分别表示N2、H2、NH3。图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是 、 。
分别表示N2、H2、NH3。图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是 、 。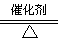 7N2+12H2O(NO也有类似的反应)
7N2+12H2O(NO也有类似的反应)