题目内容
欲验证某瓶中装的是氨水,现用一沾有浓盐酸的玻璃棒靠近瓶口,为了使现象明显,可先往瓶中加入一种物质,该物质可以选用下列物质中的( )
①浓H2SO4②固体烧碱③固体碳酸钙④生石灰⑤固体NH4Cl⑥固体食盐
①浓H2SO4②固体烧碱③固体碳酸钙④生石灰⑤固体NH4Cl⑥固体食盐
| A.①② | B.②④⑤ | C.②③④⑤ | D.①③⑥ |
B
试题分析:氨水中存在的平衡为NH3+H2O
 NH3·H2O
NH3·H2O NH4++OH-;固体烧碱溶于水放出大量的热,并使溶液中的OH-浓度增大,促使平衡逆向移动,生成氨气;生石灰溶于水放出大量的热,同时生成Ca(OH)2,促使平衡逆向移动,放出氨气;固体氯化铵溶于水,使溶液中的OH-浓度增大,促使平衡逆向移动,生成氨气,以便于检验,故B正确。
NH4++OH-;固体烧碱溶于水放出大量的热,并使溶液中的OH-浓度增大,促使平衡逆向移动,生成氨气;生石灰溶于水放出大量的热,同时生成Ca(OH)2,促使平衡逆向移动,放出氨气;固体氯化铵溶于水,使溶液中的OH-浓度增大,促使平衡逆向移动,生成氨气,以便于检验,故B正确。
练习册系列答案
相关题目
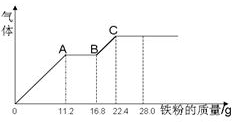
 CO2 (g)+ H2 (g) △H<0,反应达到平衡后,为提高CO的转化率,可采取的措施有 ,已知1000K时该反应的平衡常数K=0.627,若要使CO的转化率超过90%,则起始物中,c(H2O)﹕c(CO)不低于 ,
CO2 (g)+ H2 (g) △H<0,反应达到平衡后,为提高CO的转化率,可采取的措施有 ,已知1000K时该反应的平衡常数K=0.627,若要使CO的转化率超过90%,则起始物中,c(H2O)﹕c(CO)不低于 ,

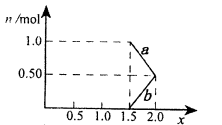
 =4,CO2的转化率随时间的变化关系如右图所示.
=4,CO2的转化率随时间的变化关系如右图所示.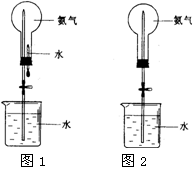
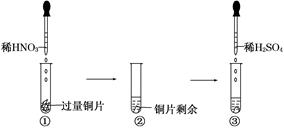

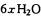 。某化学兴趣小组模拟该处理过程的实验装置如下(夹持装置已略去):
。某化学兴趣小组模拟该处理过程的实验装置如下(夹持装置已略去):