题目内容
9.可以通过丁达尔现象现象来区别溶液和胶体.能使胶体聚沉的方法(只需写出其中一种):加热、搅拌等.分析 溶液和胶体的鉴别方法利用胶体具有丁达尔现象分析,胶体聚沉的条件有加热、加入电解质溶液、加入相反电荷的胶体等.
解答 解:区别溶液和胶体的方法是胶体具有丁达尔现象,光线通过胶体出现一条光亮通路,可以鉴别溶液和胶体,胶体聚沉的原因是胶体微粒表面吸附的带电粒子,被加入物质中和,使胶体微粒聚集成更大颗粒沉淀,有加热、加入电解质溶液、加入相反电荷的胶体等方法,故答案为:丁达尔现象;加热、搅拌等.
点评 本题考查胶体的性质、分散系性质和鉴别方法,注意实质理解,掌握基础是关键,题目较简单.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案
相关题目
19.有四种氯化物,它们的通式为XCl2,其中最可能是第 IIA族元素的氯化物是( )
| A. | 白色固体,完全溶于水,得到一种无色中性溶液,此溶液导电性差 | |
| B. | 白色固体,易溶于水,得无色中性溶液,此溶液具有良好的导电性 | |
| C. | 白色固体,极易升华,如与水接触,可慢慢分解 | |
| D. | 绿色固体,易被氧化,得到一种蓝绿色溶液,此溶液具有良好的导电性 |
20.下列说法正确的是( )
| A. | 标准状况下22.4L/mol 就是气体摩尔体积 | |
| B. | 非标准状况下,1mol 任何气体的体积不可能为22.4L | |
| C. | 标准状况下22.4L 任何气体都含有约6.02×1023个分子 | |
| D. | 1mol H2 和O2 的混合气体在标准状况下的体积约为44.8L |
4.下列各组离子中,在给定条件下能够大量共存的是( )
| A. | 在加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42-、NO3- | |
| B. | 无色碱性溶液中:Na+、K+、MnO4-、CO32- | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:NH4+、Al3+、NO3-、Cl- | |
| D. | c(ClO-)=1.0 mol•L-1的溶液:Na+、SO32-、S2-、SO42- |
14.在无色透明酸性溶液中,能大量共存的离子组是( )
| A. | Mg2+、NO3-、Cl-、Na+ | B. | K+、SO42-、HCO3-、Na+ | ||
| C. | NH4+、NO3-、Al3+、CH3COO- | D. | MnO4-、K+、SO42-、Na+ |
18.化学与生产、生活密切相关.下列叙述中,不正确的是( )
①制作计算机芯片的材料是Si晶体,漂白液的有效成分是NaClO
②二氧化碳和氮气均是造成温室效应的气体
③食醋可去除水垢,NH4Cl溶液可去除铁锈
④SO2和NO2都能使雨水的pH<5.6,造成酸雨
⑤硅胶可用作食品干燥剂
⑥向FeCl3溶液中不断加入NaOH溶液制备Fe(OH)3胶体
⑦用铜粉和硫粉混合加热制备CuS
⑧向铝盐溶液中不断滴入烧碱溶液制备Al(OH)3.
①制作计算机芯片的材料是Si晶体,漂白液的有效成分是NaClO
②二氧化碳和氮气均是造成温室效应的气体
③食醋可去除水垢,NH4Cl溶液可去除铁锈
④SO2和NO2都能使雨水的pH<5.6,造成酸雨
⑤硅胶可用作食品干燥剂
⑥向FeCl3溶液中不断加入NaOH溶液制备Fe(OH)3胶体
⑦用铜粉和硫粉混合加热制备CuS
⑧向铝盐溶液中不断滴入烧碱溶液制备Al(OH)3.
| A. | ②③⑦ | B. | ②⑥⑦⑧ | C. | ②③⑦⑧ | D. | ①②③⑥⑧ |
12.用分液漏斗可以分离的一组混合物是( )
| A. | 溴苯和水 | B. | 乙酸乙酯和水 | C. | 溴乙烷和乙醇 | D. | 乙醇和水 |
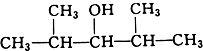 B.
B.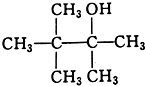
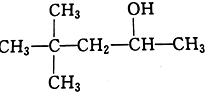 D.CH3(CH2)5CH2OH
D.CH3(CH2)5CH2OH