题目内容
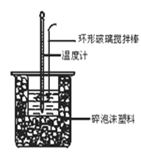
【题目】实验室制取硝基苯的方法如图所示:
(1)写出该反应的反应方程式:______,
(2)该反应中,长导管的作用是______,实验中采用如图所示的加热方式是为了____

(3)实验完成后,将试管内的物质倒入水中______.
【答案】![]() +HNO3
+HNO3![]()
![]() 冷凝、回流反应物 受热均匀,容易控制温度 冷却
冷凝、回流反应物 受热均匀,容易控制温度 冷却
【解析】
苯易发生取代反应,与浓硝酸、浓硫酸的混合酸共热时发生硝化反应生成硝基苯,该反应温度为50﹣60度,可以用水浴加热控制温度,长导管起冷凝回流作用,充分利用原料,注意苯和硝酸都是易挥发、且苯为有毒的物质,以此来解答。
(1)苯易发生取代反应,与浓硝酸、浓硫酸的混合酸共热时发生硝化反应,反应的化学方程式为![]() +HNO3
+HNO3![]()
![]() +H2O;
+H2O;
(2)该反应中,长导管的作用是冷凝、回流反应物,采用如图所示的加热方式为水浴加热,是为了受热均匀,容易控制温度;
(3)为防止苯、浓硝酸等挥发到空气中,造成污染,则实验完成后,将试管内的物质倒入水中冷却。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】草酸亚铁晶体(FeC2O4·xH2O)为淡黄色粉末,不溶于水,可作照相显影剂和制药工业,某化学兴趣小组对其性质进行如下探究。回答下列问题:
Ⅰ.定性探究
选用下列试剂设计实验方案,完成下表内容。
试剂:酸性KMnO4 溶液、H2O2 溶液、KSCN 溶液
操作 | 现象 | 结论与解释 |
(1)取少量草酸亚铁晶体于试管中,加入2mL 水,振荡后静 置 | 有淡黄色沉淀,上层清液无色 | ___________________________ |
(2)继续加入2mL稀硫酸,振荡 | 固体溶解,溶液变为浅绿色 | 草酸亚铁溶于硫酸,硫酸酸性____草酸(填“强于”、“弱于”或“等于”) |
(3)向步骤(2)所得溶液中滴加几滴K3[Fe(CN)6]溶液 | ___________ | 含有Fe2+ |
(4)________________________________ | ___________ | H2C2O4 或C2O42-具有还原性 |
Ⅱ.定量探究:滴定实验测x 的值
(5)滴定前,下列操作的正确顺序是c→ _________ →d(填字母序号)。
a.排尽滴定管尖嘴的气泡并调整液面 b.盛装0.1000 mol·L-1 的酸性KMnO4 溶液
c.查漏、清洗 d.初始读数、记录为0.50 mL
e.用0.1000 mol·L-1 的酸性KMnO4 溶液润洗
(6)称取 m 克样品,加入适量稀硫酸溶解,用步骤(5)准备的标准KMnO4 溶液直接滴定,溶解时最适合的玻璃仪器是_______________ ,滴定反应的氧化产物是________________。
(7)终点读数为20.50mL。结合上述实验数据求得x=____________(用含m 的代数式表示,FeC2O4 的相对分子质量为144)。