题目内容
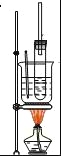
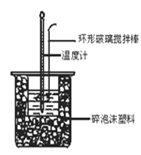
【题目】下列有关中和热概念、中和热测定实验(如图)的说法正确的是
A.已知在稀溶液中:H+(aq)+OH-(aq) =H2O(l);ΔH=-57.3kJ·mol-1,则有![]() H2SO4(aq)+
H2SO4(aq)+![]() Ba(OH)2(aq)=
Ba(OH)2(aq)= ![]() BaSO4(s)+H2O(l) △H=-57.3kJ·mol-1
BaSO4(s)+H2O(l) △H=-57.3kJ·mol-1
B.已知2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) △H=-114.6kJ·mol-1,则该反应的中和热为114.6 kJ·mol-1。
C.中和热测定实验过程中,环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小
D.酸碱混合时,量筒中的NaOH溶液应分多次倒入已装有盐酸的小烧杯中,并不断用环形玻璃搅拌棒搅拌。
【答案】C
【解析】
A.H2SO4和Ba(OH)2的反应中,除了生成水,还生成了BaSO4,故其放出的热量不是57.3kJ,还包含BaSO4的生成热,A项错误;
B.中和热是指在稀溶液中,强酸和强碱发生中和反应生成1mol水时的反应热,B项不符合中和热的定义,B项错误;
C.环形玻璃搅拌棒材料若用铜代替,会因为铜传热快而导致热量损失,致使测量的中和热数值偏小,C项正确;
D.NaOH溶液分多次倒入已装有盐酸的小烧杯中会导致热量散失,使得测量的温度差偏小,得到的中和热的数值偏小。应尽量一次快速地将NaOH溶液倒入已装有盐酸的小烧杯中,D项错误;
答案选C。

练习册系列答案
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
【题目】用如图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )
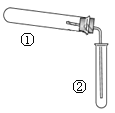
①中实验 | ②中现象 | |
Ⅰ | 铁粉与水蒸气加热 | 肥皂水冒泡 |
Ⅱ | 加热NH4Cl和Ca(OH)2混合物 | 酚酞溶液变红 |
Ⅲ | NaHCO3 | 澄清石灰水变浑浊 |
A.只有ⅠB.只有Ⅱ
C.只有ⅢD.Ⅰ、Ⅱ、Ⅲ均能证实①中反应发生