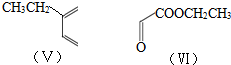
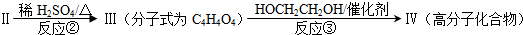题目内容
下列说法正确的是( )
| A、淀粉、蔗糖油脂的水解产物都是葡萄糖 |
| B、可以用盐析和变性来分离提纯蛋白质 |
| C、F、Cl、Br、I的氢化物的稳定性随核电荷数的增大而减弱 |
| D、酸性氧化物在常温下均为气态 |
考点:淀粉的性质和用途,元素周期律的作用,蔗糖、麦芽糖简介,氨基酸、蛋白质的结构和性质特点
专题:元素及其化合物,有机反应
分析:A.油脂是高级脂肪酸甘油酯,水解生成高级脂肪酸和甘油;
B.蛋白质的变性是不可逆的过程;
C.非金属性越强气态氢化物的稳定性越强;
D.二氧化硅属于酸性氧化物,常温下为固体.
B.蛋白质的变性是不可逆的过程;
C.非金属性越强气态氢化物的稳定性越强;
D.二氧化硅属于酸性氧化物,常温下为固体.
解答:
解:A.油脂的水解产物高级脂肪酸和甘油,得不到葡萄糖,故A错误;
B.蛋白质变性后,失去生理活性,该过程不可逆,不能用来分离提纯蛋白质,故B错误;
C.F、Cl、Br、I的非金属性随核电荷数的增大而减弱,所以氢化物的稳定性随核电荷数的增大而减弱,故C正确;
D.二氧化硅属于酸性氧化物,常温下为固体,故D错误;
故选:C.
B.蛋白质变性后,失去生理活性,该过程不可逆,不能用来分离提纯蛋白质,故B错误;
C.F、Cl、Br、I的非金属性随核电荷数的增大而减弱,所以氢化物的稳定性随核电荷数的增大而减弱,故C正确;
D.二氧化硅属于酸性氧化物,常温下为固体,故D错误;
故选:C.
点评:本题考查了常见物质的性质,题目难度不大,熟悉淀粉、蔗糖、油脂、蛋白质的性质和结构是解题关键,注意元素非金属性强弱的判断依据.

练习册系列答案
相关题目
某地有甲、乙两工厂排放污水,污水中各含有下列8种离子中的4种(两厂不含相同的离子):Ag+、Ba2+、Fe3+、Na+、SO42-、NO3-、OH-、Cl-.两厂单独排放都会造成严重的水污染,如将两厂的污水按一定比例混合,沉淀后污水便变成无色澄清的只含硝酸钠而排放,污染程度大大降低.关于污染源的分析,你认为正确的是( )
| A、SO42-和NO3- 可能来自同一工厂 |
| B、Cl-和NO3- 一定在不同的工厂 |
| C、Ag+和Na+可能来自同一工厂 |
| D、Na+和NO3- 一定不来自同一工厂 |
下列说法正确的是( )
| A、NaHSO3和NaHCO3的混合溶液中(S和C均用R表示):c(Na+)+c(H+)=c(HRO3-)+c(RO32-)+c(OH-) |
| B、常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2,三种溶液中水的电离程度:③>①>② |
| C、39g Na2O2与足量水反应后转移的电子数为NA(NA表示阿伏加德罗常数的值) |
| D、当6.9g Fe3O4与足量稀HNO3反应(还原产物只有NO),则参加反应的HNO3为0.28mol |
下列微粒在溶液中能大量共存,通入SO2后仍能大量共存的一组是( )
| A、Ba2+、Na+、H+、Cl- |
| B、Na+、K+、SO32-、Cl- |
| C、Al3+、K+、Br-、HCO3- |
| D、Fe3+、Na+、H2O2、SO42- |
下列说法中,正确的是( )
| A、对“地沟油”进行分馏可以获得汽油发动机的燃料 |
| B、乙烯和聚乙烯都可与溴水发生加成反应 |
| C、研究表明禽流感病毒H7N9在沸水中两分钟就能被杀死,是因为蛋白质受热易变性 |
| D、乙醇和乙酸的反应与苯和液溴的反应类型不同 |
常温下,在0.005mol/L H2SO4中,水的离子积是( )
| A、1×10-14 |
| B、1×10-12 |
| C、1×10-24 |
| D、1×10-4 |
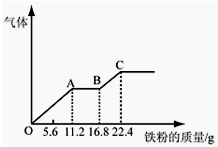 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )| A、原混合酸中NO3-物质的量浓度为2mol/L |
| B、OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 |
| C、第二份溶液中最终溶质为FeSO4 |
| D、H2SO4浓度为2.5mol?L-1 |