题目内容
20.配平化学方程式:1K2Cr2O7+14HCl--2KCl+2CrCl3+3Cl2↑+7H2O.浓盐酸在上述反应中体现的性质有AC.
A.还原性 B.氧化性 C.酸性 D.既有氧化性又有还原性.
分析 反应中氯从-1升为0价,2个氯离子共升高2价,铬元素化合价从+6降为+3,两个铬共降低6价,化合价升降最小公倍数为6,故K2Cr2O系数为1,CrCl3系数为2,Cl2系数为3,再根据元素守恒确定其它物质的系数,配平方程式,在生成KCl、CrCl3时氯的化合价不变,体现盐酸的酸性,生成Cl2体现盐酸的还原性,据此答题.
解答 解:反应中氯从-1升为0价,2个氯离子共升高2价,铬元素化合价从+6降为+3,两个铬共降低6价,化合价升降最小公倍数为6,故K2Cr2O系数为1,CrCl3系数为2,Cl2系数为3,根据K元素守恒可知KCl系数为2,根据Cl元素守恒可知HCl系数为14,根据H元素可知H2O的系数为7,反应方程式为2K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O,在生成KCl、CrCl3时氯的化合价不变,体现盐酸的酸性,生成Cl2体现盐酸的还原性,故选AC,
故答案为:1、14、2、2、3、7;AC.
点评 本题考查氧化还原反应配平,难度中等,根据化合价升降和原子守恒配平,注意掌握在该反应中HCl部分被氧化.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
11.下列关于热化学反应的描述中正确的是( )
| A. | HCl和NaOH反应的中和热△H=-57.3kJ•mol-1,则1mol H2SO4和足量氨水反应,释放的热量为114.6kJ | |
| B. | 已知在1×105Pa、298K条件下,2mol氢气燃烧生成水蒸气,放出484 kJ热量,则有:H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=+242kJ/mol | |
| C. | 燃料电池中将甲醇蒸气转化为氢气的热化学方程式是:CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H=-192.9kJ•mol-1,则CH3OH(g)的燃烧热为192.9kJ•mol-1 | |
| D. | 需要加热才能发生的反应一定是吸热反应 |
8.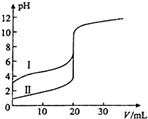 室温下,用0.100mol•L-1 NaOH溶液分别滴定20.00ml 0.100mol•L-1 的盐酸和醋酸,滴定曲线如图所示,下列说法不正确的是( )
室温下,用0.100mol•L-1 NaOH溶液分别滴定20.00ml 0.100mol•L-1 的盐酸和醋酸,滴定曲线如图所示,下列说法不正确的是( )
 室温下,用0.100mol•L-1 NaOH溶液分别滴定20.00ml 0.100mol•L-1 的盐酸和醋酸,滴定曲线如图所示,下列说法不正确的是( )
室温下,用0.100mol•L-1 NaOH溶液分别滴定20.00ml 0.100mol•L-1 的盐酸和醋酸,滴定曲线如图所示,下列说法不正确的是( )| A. | Ⅱ表示的是滴定盐酸的曲线 | |
| B. | PH=7时,滴定盐酸消耗V(NaOH)大于滴定醋酸消耗V(NaOH) | |
| C. | V(NaOH)=20ml时,C(Cl-)═C(CH3COO-) | |
| D. | V(NaOH)=10ml时,醋酸溶液中:C(CH3COO- )>C(Na+ )>C(H+)>C(OH-) |
12.下列过程中,需吸收能量的是( )
| A. | H+H→H2 | B. | 天然气燃烧 | C. | I2→I+I | D. | S+O2→SO2 |
 .
. 按如图装置进行实验,并回答下列问题
按如图装置进行实验,并回答下列问题