��Ŀ����
����Ŀ��������������ǿ�������״������DZ��ҩ���ϳ�·�����£�
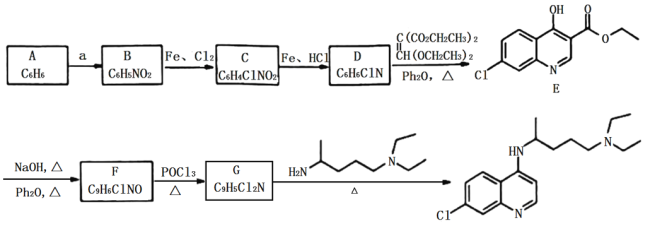
��֪�� 
![]()

(1)A��һ�ַ��������Լ�aΪ��____________________��
(2)B��Ӧ����C�ķ�Ӧ��ѧ����ʽΪ____________________��
(3)��C����D����F����G�ķ�Ӧ���ͷֱ�Ϊ__________��___________��
(4)D�Ľṹ��ʽΪ_________��
(5)E�к��������ŵ�����Ϊ________��
(6)I��E��Ϊͬ���칹�壬�Ҿ�����ȫ��ͬ�Ĺ����ţ���������������I��____�֡�(�����������칹)
�ٷ��ӽṹ�к���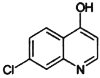 ���ڷ����л�״�ṹ��ֻ������ȡ������д�������������ֽṹ��ʽ____��______��
���ڷ����л�״�ṹ��ֻ������ȡ������д�������������ֽṹ��ʽ____��______��
(7)�л���J(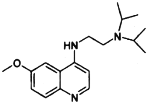 )������Ѫ���没��ҩ���������
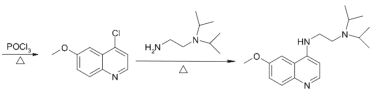
)������Ѫ���没��ҩ���������![]() �ĺϳ�·�ߣ������4-����������(
�ĺϳ�·�ߣ������4-����������( )��N��N-��������Ҷ���(
)��N��N-��������Ҷ���(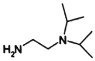 )Ϊ��ʼԭ���Ʊ��л�J�ĺϳ�·��_______________________(���Լ�����ѡ��)��
)Ϊ��ʼԭ���Ʊ��л�J�ĺϳ�·��_______________________(���Լ�����ѡ��)��
���𰸡�Ũ���� Ũ���� ![]() +Cl2
+Cl2![]()
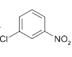 +HCl ��ԭ��Ӧ ȡ����Ӧ
+HCl ��ԭ��Ӧ ȡ����Ӧ ![]() �ǻ� ���� 30
�ǻ� ���� 30 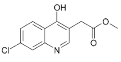
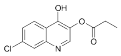
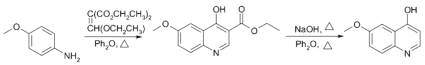
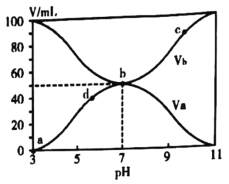
��������
AΪ ������Ũ���ᡢŨ������Һ��������B��������
������Ũ���ᡢŨ������Һ��������B��������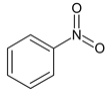 �������������������ȷ�����λȡ������C��CΪ
�������������������ȷ�����λȡ������C��CΪ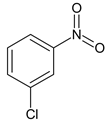 ��C����������������·�����ԭ��Ӧ����D��DΪ
��C����������������·�����ԭ��Ӧ����D��DΪ![]() ��D��
��D��![]() ��NaOH��Pt2O����������E
��NaOH��Pt2O����������E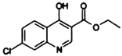 ����NaOH��Pt2O����������F��FΪ
����NaOH��Pt2O����������F��FΪ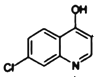 ��F��POCl2����ȡ����Ӧ��-OH��Clȡ������G��GΪ
��F��POCl2����ȡ����Ӧ��-OH��Clȡ������G��GΪ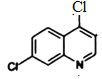 ��G��
��G��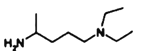 ����ȡ����Ӧ���ɲ�ƷH��HΪ
����ȡ����Ӧ���ɲ�ƷH��HΪ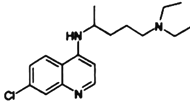 ��
��
(1)AΪ ������Ũ���ᡢŨ������Һ��������B���������Լ�aΪ��Ũ���� Ũ���ᡣ�ʴ�Ϊ��Ũ���� Ũ���
������Ũ���ᡢŨ������Һ��������B���������Լ�aΪ��Ũ���� Ũ���ᡣ�ʴ�Ϊ��Ũ���� Ũ���
(2)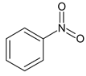 �������������������ȷ�����λȡ������C��CΪ
�������������������ȷ�����λȡ������C��CΪ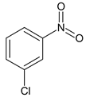 ����ѧ����ʽΪ
����ѧ����ʽΪ![]() +Cl2
+Cl2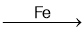
 +HCl���ʴ�Ϊ��
+HCl���ʴ�Ϊ��![]() +Cl2
+Cl2![]()
 +HCl��
+HCl��
(3)CΪ ��C����������������·�����ԭ��Ӧ����D��DΪ
��C����������������·�����ԭ��Ӧ����D��DΪ![]() ��FΪ
��FΪ ��F��POCl2����ȡ����Ӧ��-OH��Clȡ������G��GΪ
��F��POCl2����ȡ����Ӧ��-OH��Clȡ������G��GΪ ����Ӧ���ͷֱ�Ϊ��ԭ��Ӧ��ȡ����Ӧ���ʴ�Ϊ����ԭ��Ӧ����ԭ��Ӧ��ȡ����Ӧ��
����Ӧ���ͷֱ�Ϊ��ԭ��Ӧ��ȡ����Ӧ���ʴ�Ϊ����ԭ��Ӧ����ԭ��Ӧ��ȡ����Ӧ��
(4)CΪ ��C����������������·�����ԭ��Ӧ����D��D�Ľṹ��ʽΪ
��C����������������·�����ԭ��Ӧ����D��D�Ľṹ��ʽΪ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
(5)E �к��������ŵ�����Ϊ�ǻ���-OH����������-COO-�����ʴ�Ϊ���ǻ���������
�к��������ŵ�����Ϊ�ǻ���-OH����������-COO-�����ʴ�Ϊ���ǻ���������
(6)I��E ��Ϊͬ���칹�壬�Ҿ�����ȫ��ͬ�Ĺ����ţ���������������I�ٷ��ӽṹ�к���
��Ϊͬ���칹�壬�Ҿ�����ȫ��ͬ�Ĺ����ţ���������������I�ٷ��ӽṹ�к��� ���ڷ����л�״�ṹ��ֻ������ȡ������E��ȥ
���ڷ����л�״�ṹ��ֻ������ȡ������E��ȥ ����3��C��2��O��һ�������Ͷȣ���ɵĻ�����Ҫ�������������6�ֻ��ţ���M����
����3��C��2��O��һ�������Ͷȣ���ɵĻ�����Ҫ�������������6�ֻ��ţ���M���� ��6�ֿ��ܽṹΪ��
��6�ֿ��ܽṹΪ��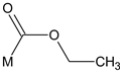 ��
��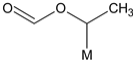 ��
��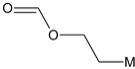 ��
��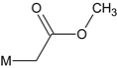 ��
��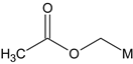 ��
�� ��ÿ�ֻ�����
��ÿ�ֻ����� ��5��λ���칹������5��6=30�������������ֽṹ��ʽ
��5��λ���칹������5��6=30�������������ֽṹ��ʽ ��
�� ��
��
�ʴ�Ϊ��30�� ��
�� ��
��
(7)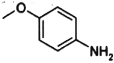 ��
��![]() ��NaOH��Pt2O����������
��NaOH��Pt2O����������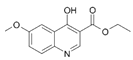 ����NaOH��Pt2O����������
����NaOH��Pt2O����������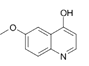 ����POCl2����ȡ����Ӧ��-OH��Clȡ������
����POCl2����ȡ����Ӧ��-OH��Clȡ������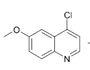 ����
����![]() ����ȡ����Ӧ���ɲ�ƷH��HΪ
����ȡ����Ӧ���ɲ�ƷH��HΪ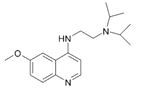 ����������
����������![]() �ĺϳ�·�ߣ������4-����������(
�ĺϳ�·�ߣ������4-����������( )��N��N-��������Ҷ���(
)��N��N-��������Ҷ���(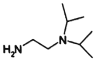 )Ϊ��ʼԭ���Ʊ��л�J�ĺϳ�·�ߣ�
)Ϊ��ʼԭ���Ʊ��л�J�ĺϳ�·�ߣ�
 ��
��
�ʴ�Ϊ��
 ��
��

 ��Ԫ������ĩ��ϵ�д�
��Ԫ������ĩ��ϵ�д�����Ŀ����ѧ��Ӧ�е������仯�����ɻ�ѧ��Ӧ�оɻ�ѧ������ʱ���յ��������»�ѧ���γ�ʱ�ų���������ͬ���¡�
��1������Ҳ�������ڹ��㻯ѧ��Ӧ�ķ�Ӧ��(��H)�±��Dz��ֻ�ѧ���ļ������ݣ�
��ѧ�� | P��P | P��O | O��O | P��O |
����/(kJ��mol��1) | 172 | 335 | 498 | X |
��֪����ȼ����Ϊ2378.0 kJ/mol��������ȫȼ�յIJ���ṹ��ͼ��ʾ�����ϱ���X��________��
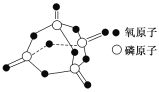
��2��1840�꣬������ѧ�Ҹ�˹�ڷ��������ѧ��Ӧ��ЧӦ�Ļ����ϣ��ܽ��һ�����ɣ���һ����ѧ��Ӧ��������һ����ɣ����Ƿּ�����ɣ����ܵ���ЧӦ����ȫ��ͬ�ģ���������ɱ���Ϊ��˹���ɣ���Щ��Ӧ�ķ�Ӧ����Ȼ��ֱ�Ӳ�ã����������ø�˹���ɼ�Ӽ�����á�
����֪��
C(ʯī)��O2(g)===CO2(g) ��H1����393.5 kJ/mol��
2H2(g)��O2(g)===2H2O(l) ��H2����571.6 kJ/mol��
2C2H2(g)��5O2(g)===4CO2(g)��2H2O(l) ��H3����2599.2 kJ/mol��
����C(ʯī)��H2(g)��Ӧ����1 mol C2H2(g)���ʱ�Ϊ__________________��
����֪3.6 g̼��6.4 g��������ȼ�գ�����Ӧ��ľ������ų�x kJ��������֪����̼��ȼ����Ϊy kJ/mol����1 mol C��O2��Ӧ����CO�ķ�Ӧ����HΪ______________��