题目内容
(2011?南京三模)钼酸钠晶体(Na2MoO4?2H2O)是无公害型冷却水系统的金属缓蚀剂,由钼精矿(主要成分是MoS2,含少量PbS等)制备钼酸钠晶体的部分流程如下:
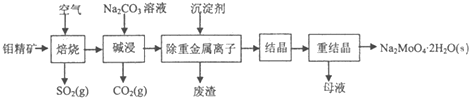
(1)写出“碱浸”反应的离子方程式:
(2)减浸液结晶前需加入Ba(OH)z固体以除去SO42-.当BaMoO4开始沉淀时,SO42-的去除率是
(3)重结晶得到的母液可以在下次重结晶时重复使用,但达到一定次数后必须净化处理,原因是
(4)如图是碳钢在3种不同介质中的腐蚀速率实验结果:
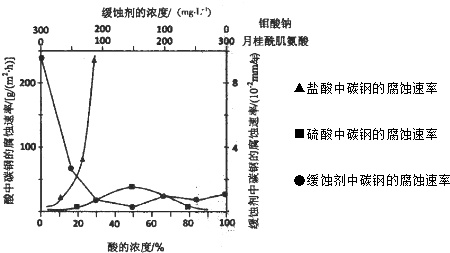
①碳钢在盐酸和硫酸中腐蚀速率随酸的浓度变化有明显差异,其原因可能是
②空气中钼酸盐对碳钢的缓蚀原理是在钢铁表面形成FeMoO4-Fe2O3保护膜.密闭式循环冷却水系统中的碳钢管道缓蚀,除需加入钼酸盐外还需加入NaNO2.NaNO2的作用是
③若缓释剂钼酸钠-月桂酸肌氨酸总浓度为300mg?L-1,则缓蚀效果最好时钼酸钠的物质的量浓度为

(1)写出“碱浸”反应的离子方程式:
MoO3+CO32-=MoO42-+CO2↑
MoO3+CO32-=MoO42-+CO2↑
(2)减浸液结晶前需加入Ba(OH)z固体以除去SO42-.当BaMoO4开始沉淀时,SO42-的去除率是
97.3%
97.3%
.[已知:碱浸液中c(MoO42-)=0.40mol?L-1,c(SO42-)=0.04mol?L-1,Ksp(BaSO4)=1.1×10-10、Ksp(BaMoO4)=4.0×10-8,加入Ba(OH)2固体引起的溶液体积变化可忽略.](3)重结晶得到的母液可以在下次重结晶时重复使用,但达到一定次数后必须净化处理,原因是
使用一定次数后,母液中杂质的浓度增大,重结晶时会析出杂质,影响产品纯度
使用一定次数后,母液中杂质的浓度增大,重结晶时会析出杂质,影响产品纯度
.(4)如图是碳钢在3种不同介质中的腐蚀速率实验结果:

①碳钢在盐酸和硫酸中腐蚀速率随酸的浓度变化有明显差异,其原因可能是
Cl-有利于碳钢的腐蚀,SO42-不利于碳钢的腐蚀,使得钢铁在盐酸中的腐蚀速率明显快
于硫酸;硫酸溶液随着浓度的增大,氧比性增强,会使钢铁钝化,腐蚀速率减慢
于硫酸;硫酸溶液随着浓度的增大,氧比性增强,会使钢铁钝化,腐蚀速率减慢
Cl-有利于碳钢的腐蚀,SO42-不利于碳钢的腐蚀,使得钢铁在盐酸中的腐蚀速率明显快
于硫酸;硫酸溶液随着浓度的增大,氧比性增强,会使钢铁钝化,腐蚀速率减慢
.于硫酸;硫酸溶液随着浓度的增大,氧比性增强,会使钢铁钝化,腐蚀速率减慢
②空气中钼酸盐对碳钢的缓蚀原理是在钢铁表面形成FeMoO4-Fe2O3保护膜.密闭式循环冷却水系统中的碳钢管道缓蚀,除需加入钼酸盐外还需加入NaNO2.NaNO2的作用是
替代空气中氧气起氧化剂作用
替代空气中氧气起氧化剂作用
③若缓释剂钼酸钠-月桂酸肌氨酸总浓度为300mg?L-1,则缓蚀效果最好时钼酸钠的物质的量浓度为
7.28×l0-4mol?L-1
7.28×l0-4mol?L-1
.分析:(1)焙烧后生成的三氧化钼与碳酸钠反应生成了MoO42-;
(2)根据钼酸呗和硫酸钡的溶度积计算出溶液中硫酸根离子的浓度,在再计算出SO42-的去除率;
(3)使用的次数较多后,母液中杂质的浓度增大,影响产品纯度;
(4)①根据图示数据分析碳钢在盐酸和硫酸中腐蚀速率随酸的浓度变化有明显差异的原因;
②根据NaNO2具有氧化性的化学性质进行分析;
③根据图象分析,在缓蚀剂中碳钢的腐蚀速率速率最小,腐蚀效果最好,最好的腐蚀效果在中点处,即钼酸钠的浓度150mg?L-1,据此计算出钼酸钠的物质的量浓度.
(2)根据钼酸呗和硫酸钡的溶度积计算出溶液中硫酸根离子的浓度,在再计算出SO42-的去除率;
(3)使用的次数较多后,母液中杂质的浓度增大,影响产品纯度;
(4)①根据图示数据分析碳钢在盐酸和硫酸中腐蚀速率随酸的浓度变化有明显差异的原因;
②根据NaNO2具有氧化性的化学性质进行分析;
③根据图象分析,在缓蚀剂中碳钢的腐蚀速率速率最小,腐蚀效果最好,最好的腐蚀效果在中点处,即钼酸钠的浓度150mg?L-1,据此计算出钼酸钠的物质的量浓度.
解答:解:(1)三氧化钼与碳酸钠反应生成了MoO42-,反应的离子方程式为:MoO3+CO32-=MoO42-+CO2↑,
故答案为:MoO3+CO32-=MoO42-+CO2↑;
(2)BaMoO4开始沉淀时,溶液中钡离子的浓度为:c(Ba2+)=
=1×10-7mol/L,
溶液中硫酸根离子的浓度为:c(SO42-)=
mol/L=1.1×10-3mol/L,
硫酸根离子的去除率为:1-
×100%=1-2.75%≈97.3%,
故答案为:97.3%;
(3)由于使用的次数较多后,母液中杂质的浓度增大,影响产品纯度,所以进行必须净化处理,
故答案为:使用一定次数后,母液中杂质的浓度增大,重结晶时会析出杂质,影响产品纯度;
(4)①由图示数据可知,碳钢在盐酸中的腐蚀速率明显快于硫酸的腐蚀速度;硫酸浓度增大变成浓硫酸后,发生了钝化现象,腐蚀速度很慢,
故答案为:Cl-有利于碳钢的腐蚀,SO42-不利于碳钢的腐蚀,使得钢铁在盐酸中的腐蚀速率明显快于硫酸;硫酸溶液随着浓度的增大,氧比性增强,会使钢铁钝化,腐蚀速率减慢;
②NaNO2的具有氧化性,能够在钢铁表面形成FeMoO4-Fe2O3保护膜,
故答案为:替代空气中氧气起氧化剂作用;
③根据图示可知,当钼酸钠、月桂酸肌氨酸浓度相等时,腐蚀速率最小,腐蚀效果最好,
所以钼酸钠的浓度为:150mg?L-1,
1L溶液中含有的钼酸钠物质的量为:
≈7.28×10-4mol,
所以钼酸钠溶液的物质的量浓度为:7.28×l0-4mol?L-1,
故答案为:7.28×l0-4mol?L-1.
故答案为:MoO3+CO32-=MoO42-+CO2↑;
(2)BaMoO4开始沉淀时,溶液中钡离子的浓度为:c(Ba2+)=
| 4.0×10-8 |
| 0.40mol?L-1 |
溶液中硫酸根离子的浓度为:c(SO42-)=
| 1.1×10-10 |
| 1×10-7 |
硫酸根离子的去除率为:1-
| 1.1×10-3 |
| 0.04 |
故答案为:97.3%;
(3)由于使用的次数较多后,母液中杂质的浓度增大,影响产品纯度,所以进行必须净化处理,
故答案为:使用一定次数后,母液中杂质的浓度增大,重结晶时会析出杂质,影响产品纯度;
(4)①由图示数据可知,碳钢在盐酸中的腐蚀速率明显快于硫酸的腐蚀速度;硫酸浓度增大变成浓硫酸后,发生了钝化现象,腐蚀速度很慢,
故答案为:Cl-有利于碳钢的腐蚀,SO42-不利于碳钢的腐蚀,使得钢铁在盐酸中的腐蚀速率明显快于硫酸;硫酸溶液随着浓度的增大,氧比性增强,会使钢铁钝化,腐蚀速率减慢;
②NaNO2的具有氧化性,能够在钢铁表面形成FeMoO4-Fe2O3保护膜,
故答案为:替代空气中氧气起氧化剂作用;
③根据图示可知,当钼酸钠、月桂酸肌氨酸浓度相等时,腐蚀速率最小,腐蚀效果最好,
所以钼酸钠的浓度为:150mg?L-1,
1L溶液中含有的钼酸钠物质的量为:
| 150×10-3g |
| 206g?mol-1 |
所以钼酸钠溶液的物质的量浓度为:7.28×l0-4mol?L-1,
故答案为:7.28×l0-4mol?L-1.
点评:本题考查了制备钼酸钠晶体的方法,注意分析题中图示是解题关键,最后一问有一定的难度,容易出错,需要合理应用题中数据,本题难度中等.

练习册系列答案
相关题目

 (2011?南京三模)核能源已日益成为当今世界的主要能源.
(2011?南京三模)核能源已日益成为当今世界的主要能源.