题目内容
下列离子方程式书写正确的是
| A.NaAlO2溶液中通入过量的CO2:2AlO2–+3H2O+CO2=2Al(OH)3+CO32– |
| B.明矾溶液中滴加Ba(OH)2溶液至SO42–恰好完全沉淀:Al3++Ba2++ SO42–+3OH–=BaSO4+Al(OH)3 |
| C.200 mL 2 mol·L–1的FeBr2溶液中通入11.2 L标准状况下的氯气:4 Fe2++6Br–+5Cl2=4Fe3++3Br2+ 10Cl– |
| D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO–+2Fe(OH)3=2FeO42–+3Cl–+H2O+4H+ |
C
解析试题分析:A、过量CO2可与CO32–反应生成HCO3–,最终产物应为HCO3–而不是CO32–,错误;B、明矾[KAl(SO4)2]溶液中Al3+与SO42–的物质的量之比为1:2,当加入2mol Ba(OH)2把2mol SO42–恰好完全沉淀时,则4molOH–与1mol Al3+反应生成AlO2–,最终产物应为AlO2–而不是Al(OH)3,错误;C、n(FeBr2)=0.4mol,n(Cl2)=0.5mol,则n(FeBr2) :n(Cl2) = 4:5,又因氧化性:Cl2>Br2>Fe3+,根据得失电子守恒可知,5molCl2可氧化4mol的Fe2+和6molBr–,故离子方程式为:4 Fe2+ + 6Br– + 5Cl2 = 4Fe3+ + 3Br2 + 10Cl–,正确;D、强碱性溶液中,H+与OH–反应生成水,错误。
考点:考查离子方程式的书写。

练习册系列答案
相关题目
下列离子方程式正确的是( )
| A.足量的CO2通入饱和碳酸钠溶液中: CO2+CO32-+H2O→2HCO3- |
B.FeSO4溶液在空气中变质:4Fe2++O2+2H2O 4Fe3++4OH- 4Fe3++4OH- |
| C.次氯酸钙溶液中通入足量二氧化硫:Ca2++ClO-+SO2+H2O→CaSO4↓+Cl-+2H+ |
| D.碳酸氢镁溶液中加入过量石灰水 Mg2++2HCO3-+2Ca2++4OH— ®2CaCO3↓+ Mg(OH)2↓+ 2H2O |
下列说法正确的是( )
| A.BaSO4在水中很难导电,所以BaSO4是非电解质 |
| B.氨气溶于水得到的氨水能导电,所以氨水是电解质 |
| C.固态的离子化合物不导电,熔融态的离子化合物能导电 |
| D.强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 |
在指定的条件下,下列各组微粒一定能大量共存的是 ( )
| A.溶有大量SO2的溶液中:Ba2+、NO3-、Na+、Cl- |
| B.酸性K2Cr2O7溶液中:C2H5OH、S2-、SO42-、K+ |
| C.室温下,C(H+)="1×10-13" mol·L-1的溶液中:NO3-、Cl-、SO32-、Na+ |
| D.遇K3[Fe(CN)6]得蓝色沉淀的溶液中:AlO2-、NH4+、Ba2+、SCN- |
下列相关反应的离子方程式书写正确的是( )
| A.氢氧化铁溶于氢碘酸:Fe(OH)3 +3H+ =Fe3++3H2O |
| B.NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3—+Ba2++2OH— = BaCO3â +2H2O+CO32— |
| C.NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
| D.向含有0.4 mol FeBr2的溶液中通入0.1 mol Cl2反应:2Fe2++Cl2=2Fe3+ +2Cl- |
常温下,下列各组离子在指定溶液中可能大量共存的是
| A.0.1mol/LNaHSO4溶液中: K+ NH4+ HCO3— NO3— |
| B.与铝反应产生氢气的溶液中:Na+ NH4+ SO42—、 CH3COO— |
| C.滴加酚酞显红色的溶液中: Na+ NO3— SO42— CO32— |
| D.NaNO3溶液中: Fe2+ H+ Cl— I— |
下列反应的离子方程式书写正确的是( )
| A.过量铁加入到稀硝酸中: 3Fe + 8H+ + 2NO3- = 3Fe2+ + 2NO↑ + 4H2O |
| B.向NaAlO2溶液中通入过量CO2: 2AlO2- + CO2+ H2O = 2Al(OH)3↓+ HCO3- |
| C.向AgC1悬浊液中滴加饱和NaI溶液: AgC1+I- ="AgI" + C1- |
| D.向KHCO3溶液中加入过量的澄清石灰水:2HCO3-+ Ca2++2OH-=CaCO3↓+CO32-+2H2O |
下列离子方程式书写正确的是 ( )
| A.向氧化铁中加入氢碘酸:Fe2O3+6H++2I-=2Fe2++I2+3H2O |
| B.Cu片插入FeCl3溶液中:Cu+Fe3+=Fe2++Cu2+ |
C.向Al2(SO4)3溶液中加入过量的氨水:Al3++4NH3·H2O=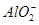 +4 +4 +2H2O +2H2O |
D.向NaHSO4溶液中滴加Ba(OH)2溶液至中性:H++ +Ba2++OH-=BaSO4↓+H2O +Ba2++OH-=BaSO4↓+H2O |
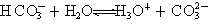
 2NH3 (g) △H=-38.6kJ·mol-1
2NH3 (g) △H=-38.6kJ·mol-1