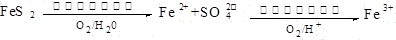题目内容
有关海洋中部分资源的利用(如图)的说法不正确的是
| A.工业上利用Cl2与澄清石灰水反应制取漂白粉 |
| B.用MgCl2·6H2O晶体制无水MgCl2,需在HCl气流中加热脱水 |
| C.SO2水溶液吸收Br2的化学方程式为:Br2+SO2+2H2O=H2SO4+2HBr |
| D.粗碘中混有少量HCl和IBr可加入KI进行升华提纯 |
A
解析试题分析:A、工业上利用Cl2与石灰乳反应制取漂白粉,石灰水浓度太小,错误;B、HCl气流中加热脱水抑制MgCl2水解,正确;C、正确;D、IBr(I为+1)与KI(I为-1)发生归中反应生成碘单质,故可以升华提纯,正确。
考点:考查元素化合物的转化有关问题。

练习册系列答案
相关题目
仅通过物理方法就能从海水中获得的物质是( )
| A.钠、镁 | B.溴、碘 | C.食盐、淡水 | D.氯气、烧碱 |
地壳中含量居第二位的非金属元素是
| A.铁 | B.铝 | C.氧 | D.硅 |
大气中CO2含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境。某研究小组在实验室测得不同温度下(T1,T2)海水中CO32-浓度与模拟空气中CO2浓度的关系曲线。下列说法不正确的是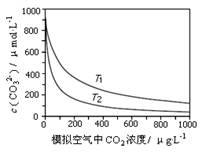
| A.T1>T2 |
| B.海水温度一定时,大气中CO2浓度增加,海水中溶解的CO2随之增大,导致CO32-浓度降低 |
| C.当大气中CO2浓度确定时,海水温度越高,CO32- 浓度越低 |
| D.大气中CO2含量增加时,海水中的珊瑚礁将逐渐溶解 |
下列是部分矿物资源的利用及产品流程(如图),有关说法不平确的是
| A.粗铜电解精炼时,粗铜作阳极 |
| B.生产铝、铜、高纯硅及玻璃过程中都涉及氧化还原反应 |
| C.黄铜矿冶铜时,副产物SO2可用于生产硫酸,FeO可用作冶铁的原料 |
| D.粗硅制高纯硅时,提纯四氯化硅可用多次分馏的方法 |
海水资源丰富,海水淡化问题已成为科学家的主要研究方向,若实行海水淡化来供应饮用水,下列方法不正确的是 ( )
| A.利用太阳能,将海水蒸馏淡化 |
| B.加入明矾,使海水的盐份沉淀并淡化 |
| C.通直流电,采用电渗透法使海水淡化 |
| D.通过离子交换膜,除去所含的盐分使海水淡化 |
下列关于硫酸工业生产过程的叙述错误的是( )
| A.在接触室中使用铁粉作催化剂 |
| B.在接触室中运用热交换技术可充分利用能源 |
| C.把硫铁矿磨成细粉末,可以提高原料的利用率 |
| D.该反应采用450~500°C主要是因为该温度下催化剂活性好 |
NaCl是海水中含量最多的盐,除食用外,它还是海洋化学工业原料,下列以NaCl为原料的产品(或物质)是( )
①烧碱 ②纯碱 ③金属钠 ④氯气 ⑤盐酸
| A.全部 | B.只有①②③④ |
| C.只有①②③⑤ | D.只有①②④⑤ |