��Ŀ����
����Ŀ����������һ����Ҫ�Ļ����м��壬������ҵ�о����ȵ㡣һ����ʯ�ͻ����еķ�������(��Ҫ�ɷ�ΪNiCO3��SiO2������������Fe2O3��Cr2O3)Ϊԭ���Ʊ��������Ĺ�ҵ������ͼ��

��֪����NiS��Ni(OH)2��Cr(OH)3��������ˮ��Cr(OH)3�������������
��Fe(OH)3������NH4Cl-��ˮ�Ļ��Һ��Ni(OH)2����NH4Cl��ˮ�Ļ��Һ����[Ni(NH3)6]2+��
��ش��������⣺
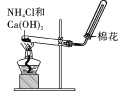
(1)��������ʱΪ�ӿ췴Ӧ���ʣ������Ԫ�صĽ����ʣ����Բ�ȡ�Ĵ�ʩ�У�________��
(2)��������������Ҫ�ɷ�Ϊ__���ѧʽ�����������ڹ�ҵ�ϵ���;Ϊ_________����дһ�֣���
(3)��һ�μ�����ʱ�������NaOH��Һ���������Ŀ����_________��
(4)��������������Ӧ�����ӷ���ʽΪ________����������ʱͨ��H2S��Ŀ����_______��
(5)��������ʱ������Ӧ�Ļ�ѧ����ʽΪ_________��
(6)��ϵ�в�����������ָ_________�����ˡ�ϴ�ӡ����
���𰸡��������������飬��20%�����ڼ��������·�Ӧ�����Ͻ���� SiO2 �Ʋ���(���ƹ��ά) ʹCr3+ת��ΪCrO2-����ȥ������ Ni(OH)2+6NH3 H2O=[Ni(NH3)6]2++2OH-+6H2O ����Ԫ��ת��ΪNiS���� 3NiS+8HNO3=3Ni(NO3)2+2NO��+3S+4H2O ����Ũ������ȴ�ᾧ
��������
��������(��Ҫ�ɷ�ΪNiCO3��SiO2��������Fe2O3��Cr2O3)Ϊԭ���Ʊ�������������20%���������ܡ����ˣ�������ΪSiO2����Һ����NaOH��Һ����һ�μ�������Һ����CrO2-�����������Ȼ�李���ˮ����Һ������Ϣ�ڿ�֪������Ϊ�������������˵õ�����Һ����[Ni(NH3)6]2+����������ʱ�����H2S������Ԫ��ת��ΪNiS��������������������������S��Ni2+������������������Ni(OH)2�����˺��������ɵõ���������������Ũ�ȡ���ȴ�ᾧ�õ����壬�Դ˽����⡣
(1)��������ʱΪ�ӿ췴Ӧ���ʣ������Ԫ�صĽ�����Ӧ�Ƚ������������飬�������������������20%������100���·�Ӧ2Сʱ�����ȿ�����Ӧ���ʣ��ύ�����ʣ�
(2)NiCO3��Fe2O3��Cr2O3���������ᣬSiO2���������ᣬ��������������Ҫ�ɷ�ΪSiO2����ҵ�Ͽ�����SiO2�Ʋ������ƴֹ衢�ƹ��ά�ȣ�
(3) Ni(OH)2��Cr(OH)3��������ˮ��Cr(OH)3������������������������������ƣ��ᷢ��Cr3++4OH-=CrO2-+2H2O��ʹCr3+ת��ΪCrO2-����ȥ��������
(4)Fe(OH)3������NH4Cl-��ˮ�Ļ��Һ��Ni(OH)2����NH4Cl-��ˮ�Ļ��Һ����[Ni(NH3)6]2+���Ӷ�ʵ����Ԫ�غ���Ԫ�صķ��룬��Ӧ����ʽΪ��Ni(OH)2+6NH3 H2O=[Ni(NH3)6]2++2OH-+6H2O����������ʱͨ��H2S��Ŀ���ǽ���Ԫ��ת��ΪNiS������
(5)ϡHNO3����ǿ�������ԣ��ὫNiS����ΪNi(NO3)2 ��S���ʣ����ᱻ��ԭΪNO������ݵ����غ㡢ԭ���غ㣬�ɵ���������ʱ������Ӧ�Ļ�ѧ����ʽ3NiS+8HNO3=3Ni(NO3)2+2NO��+3S+4H2O��
(6)��NiSO4��Һ�л��NiSO47H2O�IJ���Ϊ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ����