题目内容
3.已知H2C2O4是二元弱酸,NaHC2O4溶液显酸性.25℃时,将a mol•L-1H2C2O4溶液与b mol•L-1NaOH溶液等体积混合(0<a≤0.1,0<b≤0.1),下列有关溶液中微粒的物质的量浓度关系正确的是( )| A. | a=b时,c(H2C2O4)+c(H+)=c(C2O42-)+c(OH-) | |
| B. | a=$\frac{b}{2}$时,c(C2O42-)>c(HC2O4-)>c(H2C2O4)>c(OH-) | |
| C. | a=2b时,2c(Na+)=c(H2C2O4)+c(HC2O4-)+c(C2O42-) | |
| D. | a=3b时,c(Na+)+c(H+)=c(HC2O4-)+c(C2O42-)+c(OH-) |
分析 NaHC2O4溶液显酸性,说明HC2O4-电离程度大于HC2O4-水解程度,
A.a=b时,二者恰好反应生成NaHC2O4,结合电荷守恒和物流守恒判断;
B.a=$\frac{b}{2}$时,二者恰好反应生成Na2C2O4,溶液中存在C2O42-和HC2O4-的两种离子的水解;
C.a=2b时,H2C2O4过量,结合物料守恒判断;
D.a=3b时,H2C2O4过量,结合电荷守恒判断.
解答 解:NaHC2O4溶液显酸性,说明HC2O4-电离程度大于HC2O4-水解程度,
A.a=b时,二者恰好反应生成NaHC2O4,溶液存在电荷守恒,为c(Na+)+c(H+)=c(HC2O4-)+2c(C2O42-)+c(OH-),存在物料守恒,为c(Na+)=c(H2C2O4)+c(HC2O4-)+c(C2O42-),二者联式可得c(H2C2O4)+c(H+)=c(C2O42-)+c(OH-),故A正确;
B.a=$\frac{b}{2}$时,二者恰好反应生成Na2C2O4,溶液中存在C2O42-和HC2O4-的两种离子的水解,则c(OH-)>c(H2C2O4),故B错误;
C.a=2b时,H2C2O4过量,反应后溶液中存在H2C2O4、HC2O4-、C2O42-,其物质的量之和为Na+的2倍,则2c(Na+)=c(H2C2O4)+c(HC2O4-)+c(C2O42-),故C正确;
D.a=3b时,H2C2O4过量,溶液存在电荷守恒,为c(Na+)+c(H+)=c(HC2O4-)+2c(C2O42-)+c(OH-),故D错误.
故选AC.
点评 本题考查离子浓度大小的比较,为高考常见题型和高频考点,侧重于学生的分析能力的考查,注意把握盐类水解与弱电解质的电离特点和影响因素,结合电荷守恒、物料守恒解答该题,难度中等.

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案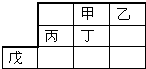
| A. | 最高价氧化物水化物的酸性:乙>丁 | |
| B. | 甲的一种单质是自然界最硬的物质 | |
| C. | 戊元素位于第4周期第 VⅢ族 | |
| D. | 乙、丙的最高价氧化物的水化物可以反应 |
| A. | Ba2+对人体无害,可用BaSO4做钡餐造影剂 | |
| B. | 海水提镁和海水提溴都涉及氧化还原反应 | |
| C. | 大量燃烧含硫的化石燃料是形成酸雨的主要原因 | |
| D. | 航天飞机上的陶瓷防护片属于新型无机非金属材料 |
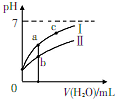 已知下表为250C时某些弱酸的电离平衡常数.如图表示常温时,稀释CH3COOH.HC1O两种酸的稀溶液时,溶液pH随加水量的变化.依据所给信息,下列说法正确的是( )
已知下表为250C时某些弱酸的电离平衡常数.如图表示常温时,稀释CH3COOH.HC1O两种酸的稀溶液时,溶液pH随加水量的变化.依据所给信息,下列说法正确的是( )| CH3COOH | HClO | H2CO3 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7 Ka2=4.7×10-11 |
| A. | 向NaCl0溶液中通人少量二氧化碳的离子方程式为:2C1O-+CO2+H2O=2HClO+CO32- | |
| B. | 相同浓度的CH3COONa和NaClO的混合溶液中,各离子浓度的大小关系是:c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) | |
| C. | a、b、c三点所示溶液中水的电离程度:c>a>b | |
| D. | 图象中,I表示CH3COOH,Ⅱ表示HC1O,且溶液导电性:c>b>a |
| A. | 生活中钢铁制品生锈主要是由于吸氧腐蚀所致 | |
| B. | 冰箱中使用的含氟制冷剂泄漏后,会增加空气中PM 2.5的含量 | |
| C. | 氯气和活性炭均可作为漂白剂,同时使用可增强漂白效果 | |
| D. | 明矾[KAl(SO4)2•12H2O]溶于水会形成胶体,因此可用于自来水的杀菌消毒 |
| A. |  滴加液体 | B. | 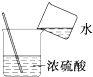 稀释浓硫酸 | C. |  检查气密性 | D. | 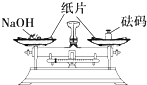 称量NaOH固体 称量NaOH固体 |
| A. | 足量铁在氯气中反应,1mol铁失去的电子数为2NA | |
| B. | 标准状况下22.4LH2中含中子数为2NA | |
| C. | NaBH4是一种重要的储氢载体,1molNaBH4与水反应[NaBH4+2H2O=NaBO2+4H2↑]时转移的电子数目为8NA | |
| D. | 常温下,1L0.2mol/L的盐酸溶液通人氨气当溶液pH=7,则溶液中NH4+数为0.2NA |
| A. | 使用节水型马桶 | B. | 生活污水任意排放 | ||
| C. | 合理使用农药和化肥 | D. | 工业废水处理达标后排放 |
 .合成M的一种途径如下:
.合成M的一种途径如下: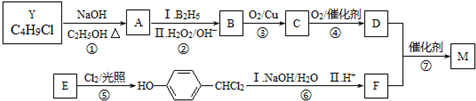
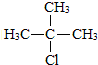 .
. .
.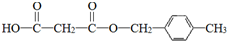 .
.