题目内容
1.以下各项中的物质,互为同分异构体的是( )| A. | CO和CO2 | B. | 淀粉和纤维素 | C. | 红磷和白磷 | D. | CH3CH2CH2CH3和 |
分析 具有相同分子式而结构不同的化合物互为同分异构体,抓住同分异构体的三要素:相同分子式、不同结构、化合物.
解答 解:A.二氧化碳和一氧化碳为碳的不同氧化物,二者的分子式不同,不属于同分异构体,故A错误;
B.淀粉和纤维素都属于混合物,二者的分子式不同,不属于同分异构体,故B错误;
C.红磷和白磷都是单质,二者互为同素异形体,故C错误;
D.CH3CH2CH2CH3和 具有相同分子式、不同结构,二者互为同分异构体,故D正确;
具有相同分子式、不同结构,二者互为同分异构体,故D正确;
故选D.
点评 本题考查了同分异构体的判断,题目难度不大,明确同位素、同分异构体、同位素、同素异形体的概念为解答关键,注意把握好同分异构体的三要素相同分子式、不同结构、化合物.

练习册系列答案
相关题目
11.下列物质属于同系物的是( )
| A. | CH2=CH-CH2-CH3和 | B. |  与 与 | ||
| C. | 分子组成都为 CnH2nO2 的物质 | D. | CH3CH2Cl与CH3CH2CH2Cl |
12.利用图装置电解饱和食盐水,下列说法正确的是( )


| A. | 电解质溶液中Cl-向a电极迁移 | |
| B. | 该装置能将化学能转变成电能 | |
| C. | b电极上发生氧化反应 | |
| D. | 若b为铁,则b电极的反应式为:Fe-2e-═Fe2+ |
6.硫酸工业中的一个反应为2SO2+O2$?_{△}^{催化剂}$2SO3,有关该反应的下列说法中正确的是( )
| A. | O2充足时,SO2可全部转化为SO3 | |
| B. | 加入催化剂是为了加快反应速率 | |
| C. | 达到化学平衡时SO2和SO3的浓度相等 | |
| D. | 达到化学反应限度时,反应停止进行 |
13.下列溶液中各微粒的浓度关系正确的是( )
| A. | 0.2mol•L-1某一元弱酸HA溶液和0.1mol•L-1NaOH溶液等体积混合后的溶液:2c(OH-)+c(A-)═2c(H+)+c(HA) | |
| B. | c(NH4+)相等的(NH4)2C03、(NH4)2S04和(NH4)2Fe(S04)2三份溶液中,溶质物质的量浓度依 次增大 | |
| C. | 在 0.lmol•L-1Na2CO3溶液中:c(OH-)-c(H+)═c(HCO3-)+c(H2C03) | |
| D. | 常温下,CH3COONa和 CH3COOH 混合溶液[pH=7,c(Na+)=0.1mol•L-1];c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-) |
10.现有下列短周期元素相关性质的数据:
试回答下列问题:
(1)元素⑤在周期表中的位置第三周期ⅦA族;
(2)元素④与元素⑦相比较,气态氢化物较稳定的是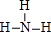 (填结构式);
(填结构式);
(3)元素④形成的+3和+5价的氯化物中,各原子均达到8电子稳定结构的化合物是PCl3(写化学式);
(4)以下叙述正确的是A.
A.氢化物的沸点为④<⑦B.①与②形成的化合物具有两性
C.与稀盐酸反应单质②比单质⑥快 D.最高价氧化物对应水化物的碱性③>⑥
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 |
| 最高正化合价 | +2 | +1 | +5 | +7 | +1 | +5 | |
| 最低负化合价 | -2 | -3 | -1 | -3 |
(1)元素⑤在周期表中的位置第三周期ⅦA族;
(2)元素④与元素⑦相比较,气态氢化物较稳定的是
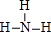 (填结构式);
(填结构式);(3)元素④形成的+3和+5价的氯化物中,各原子均达到8电子稳定结构的化合物是PCl3(写化学式);
(4)以下叙述正确的是A.
A.氢化物的沸点为④<⑦B.①与②形成的化合物具有两性
C.与稀盐酸反应单质②比单质⑥快 D.最高价氧化物对应水化物的碱性③>⑥
11.化学是社会生活联系最为紧密的学科之一,下列有关化学与生活说法错误的是( )
| A. | 利用石油中各组分沸点的不同,通过分馏的方法可以获得汽油、煤油、柴油 | |
| B. | 不加糖不等于没有糖,糖尿病人应该注意日常饮食 | |
| C. | 水果散发出诱人的香味,其主要成分是一种低级酯类物质 | |
| D. | 煤的干馏属于物理变化 |
 .
.