题目内容
【题目】下列说法正确的是
A.二氧化硅溶于水显酸性B.二氧化碳通入Na2SiO3溶液中可以得到硅酸
C.二氧化硅常用作干燥剂D.二氧化硅是酸性氧化物,它不溶于任何酸
【答案】B
【解析】
A.二氧化硅属于酸性氧化物但和水不反应,故A错误;
B.碳酸酸性大于硅酸,所以二氧化碳、水和硅酸钠反应生成原硅酸,故B正确;
C.二氧化硅没有吸水性,不能做干燥剂,作干燥剂的是硅胶,故C错误;
D.二氧化硅属于酸性氧化物,能溶于强碱溶液,且能溶于HF,所以可以用HF雕刻玻璃,故D错误;
答案选B。

 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案【题目】下表列出了A~R 10种元素在周期表中的位置(填元素符号):
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | E | J | F | |||||
3 | A | C | D | G | R | |||
4 | B | H |
i. 请填空:
(1)这10种元素中,化学性质最不活泼的是____(填元素符号)。
(2)D元素最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是____。
(3)A、B、C三种元素按原子半径由大到小的顺序排列为____(填元素符号)。
(4)EF2的电子式为____,F元素的最简单氢化物在常温下跟B发生反应的化学方程式是____。
(5)G元素和H元素两者核电荷数之差是____。
ii. 元素J的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2。某同学在实验室中对NH3与NO2反应进行了探究。回答下列问题:
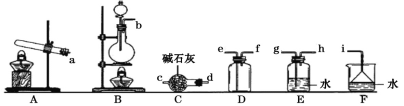
①只用固体药品制备氨气的发生装置可以选择上图中的____,反应的化学方程式为____。
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→____(按气流方向,用小写字母表示)。
③将上述收集到的NH3充入无色透明烧瓶中,并加入少量催化剂,然后充入NO2。常温下反应一段时间后的实验现象为____,反应的化学方程式为____。