题目内容
3.下列化学式能真实表示物质分子组成的是( )| A. | NaOH | B. | CO2 | C. | C | D. | SiO2 |
分析 化学式能真实表示物质分子组成的是分子晶体,常见的分子晶体有:所有非金属氢化物、部分非金属单质(金刚石、晶体硅等除外)、部分非金属氧化物(二氧化硅等除外)、几乎所有的酸、绝大多数的有机物晶体,据此进行判断.
解答 解:A.NaOH为离子化合物,只有钠离子和氢氧根离子,没有分子,故A错误;
B.CO2为非金属氧化物,属于分子晶体,晶体中只存在分子,能用CO2能表示物质分子组成,故B正确;
C.C为碳原子,无论石墨、金刚石还是碳单质,都不存在分子,故C错误;
Si02为原子晶体,是由硅原子和氧原子以共价键构成的空间网状结构,没有Si02分子,故D错误.
故选B.
点评 本题考查物质组成与化学式的关系,题目难度不大,试题侧重于学生的分析能力的考查,掌握常见物质晶体类型及常见分子晶体是解答的关键.

练习册系列答案
相关题目
13.下表是元素周期表的一部分,回答下列问题:(请用元素符号或化学式回答)
(1)在这些元素中,与水反应最剧烈的金属元素是Na;元素的气态氢化物最稳定的物质是HF.
(2)这些元素的最高价氧化物的对应水化物中HClO4酸性最强;NaOH碱性最强;
(3)⑤、⑦的最高价氧化物的对应水化物发生反应的化学方程式Al(OH)3+NaOH═NaAlO2+2H2O
(4)②形成单质的结构式N≡N;①和③形成的酸性氧化物的电子式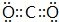 ;
;
(5)在这些元素中,原子半径最大的非金属元素的原子是Si.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | VⅡA | O |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(2)这些元素的最高价氧化物的对应水化物中HClO4酸性最强;NaOH碱性最强;
(3)⑤、⑦的最高价氧化物的对应水化物发生反应的化学方程式Al(OH)3+NaOH═NaAlO2+2H2O
(4)②形成单质的结构式N≡N;①和③形成的酸性氧化物的电子式
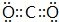 ;
;(5)在这些元素中,原子半径最大的非金属元素的原子是Si.
11.关于下列各装置的叙述不正确的是( )
| A. |  如图装置可用于制备乙酸乙酯 | |
| B. |  如图装置可用于模拟海水蒸馏 | |
| C. |  如图装置可用于探究碳酸氢钠的热稳定性 | |
| D. |  如图装置为配制溶液过程中的定容操作 |
15.世界气候大会与2009年在丹麦首都哥本哈根召开,商讨2012年至2020年全球温室气体减排协议.下列物质属于温室气体的是( )
| A. | 可吸入颗粒 | B. | 氮气 | C. | 氧气 | D. | 二氧化碳 |
12.观察图:对合成氨反应中,下列叙述错误的是( )


| A. | 开始反应时,正反应速率最大,逆反应速率为零 | |
| B. | 随着反应的进行,正反应速率逐渐减小,逆反应速率逐渐增大 | |
| C. | 反应到达t1时,正反应速率与逆反应速率相等,反应停止 | |
| D. | 反应在t1之后,正反应速率与逆反应速率相等,反应达到化学平衡状态 |
13.下列化合物中,既有离子键,又有共价键的是( )
| A. | NH3 | B. | KOH | C. | CaCl2 | D. | H2O |
 .
. 如图为某化学兴趣小组设计的乙醇氧化的实验装置(图中加热仪器、铁架台、铁夹等均未画出).图中:A为无水乙醇(沸点为78℃),B为绕成螺旋状的细铜丝或银丝,C为无水CuSO4粉末,D为碱石灰,F为新制的碱性Cu(OH)2悬浊液.
如图为某化学兴趣小组设计的乙醇氧化的实验装置(图中加热仪器、铁架台、铁夹等均未画出).图中:A为无水乙醇(沸点为78℃),B为绕成螺旋状的细铜丝或银丝,C为无水CuSO4粉末,D为碱石灰,F为新制的碱性Cu(OH)2悬浊液.