题目内容
17. 某同学利用家中废旧材料制作一个可使玩具扬声器发出声音的电池、装置如图所示.下列说法正确的是( )
某同学利用家中废旧材料制作一个可使玩具扬声器发出声音的电池、装置如图所示.下列说法正确的是( )| A. | 碳棒上发生的主要反应为:2H++2e-═H2↑ | |
| B. | 铝质易拉罐作为电池的正极 | |
| C. | 电池总反应为:4Al+3O2+6H2O═4Al(OH)3 | |
| D. | 电流流动方向为:铝质易拉罐→导线→扬声器→导线→碳棒→浸透食盐水的布 |
分析 该装置构成原电池,铝易失电子作负极,碳作正极,负极上铝失电子发生氧化反应,正极上氧气得电子发生还原反应,据此分析解答.
解答 解:A.碳棒上氧气得电子发生还原反应,电极反应式为:O2+2H2O+4e-=4OH-,故A错误;
B.铝作负极,负极上铝失电子生成铝离子而被腐蚀,故B错误;
C.负极上铝失电子发生氧化反应生成铝离子,正极上氧气得电子发生还原反应生成氢氧根离子,铝离子和氢氧根离子反应生成氢氧化铝,所以电池反应式为4Al+3O2+6H2O═4Al(OH)3,故C正确;
D.电子不进入电解质溶液,故D错误;
故选C.
点评 本题考查了金属的腐蚀,明确原电池原理是解本题关键,根据电解质溶液酸碱性确定发生的腐蚀,难点是电极反应式的书写,要结合电解质的性质书写,易错选项是D,注意电子不进入电解质溶液,电解质溶液中是通过离子的定向移动而形成电流的,为易错点.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
7.某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )
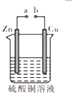

| A. | a和b不连接时,锌片上会有紫红色固体析出 | |
| B. | a和b用导线连接时,铜片上的电极反应是Cu2++2e-→Cu | |
| C. | a和b用导线连接时,溶液的颜色加深 | |
| D. | 无论a和b是否连接,锌片均会溶解 |
5.乙醇分子中不同的化学键,如图:关于乙醇在各种反应中断裂键的说法不正确的是( )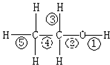

| A. | 乙醇和钠反应,键①断裂 | B. | 铜催化下和O2反应,键①③断裂 | ||
| C. | 乙醇与乙酸反应,键①断裂 | D. | 铜催化和O2反应,键①②断裂 |
2.下列有关物质的性质与应用相对应的是( )
| A. | 碳酸钠溶液呈碱性,可用于洗去铁屑表面的油污 | |
| B. | 浓硫酸具有强氧化性,可用于与亚硫酸钠反应制取二氧化硫 | |
| C. | 氢氧化铝能表现弱酸性,可用于制抗酸药品 | |
| D. | 铜的金属活动性比铁的弱,可在海轮外壳上装若干铜块以减缓船体腐蚀速率 |
9.下列各组物质中,所含分子数一定相同的是( )
| A. | 1gH2和8gO2 | |
| B. | 0.1molHCl和2.24LHe | |
| C. | 150℃,1.01×105Pa时,18LH2O和18LCO2 | |
| D. | 常温常压下28gCO和6.02×1022个CO分子 |
6.某反应由两步反应A?B?C构成,它的反应能量曲线如图,下列叙述正确的是( )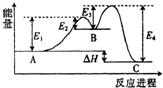

| A. | 两步反应均为吸热反应 | B. | 三种化合物中C最稳定 | ||
| C. | 加入催化剂会改变反应的反应热 | D. | A?B反应,反应条件一定要加热 |
 A、B、C、D、E是中学化学常见的物质.其中,A、B是短周期元素组成的非金属单质,C是金属单质,D是无色液体.其转化关系如下:
A、B、C、D、E是中学化学常见的物质.其中,A、B是短周期元素组成的非金属单质,C是金属单质,D是无色液体.其转化关系如下: