��Ŀ����
����Ŀ����֪A��B��C��D��E Ϊԭ���������������ǰ������Ԫ�ء���֪ǰ����Ԫ�صĻ�̬ԭ��p�ܼ�����2�������ӣ�E ��ԭ����������A��B��C����Ԫ��ԭ������֮�͡�
�Իش���������:
(1)��̬Eԭ����Χ�����Ų�ͼΪ_________������M �ܲ���_____��������ͬ�ĵ��ӡ�
(2)��ԭ�ӽṹ�ǶȽ���B �縺�Դ���D��ԭ����:_______________��
(3) ��AԪ�صĻ������У�A ��ԭ�Ӽ䳣�Цм������Ǻ�CԪ�صĻ������У�C��ԭ�Ӽ�ֻ�ܴ��ڦҼ�������Ҫԭ����___________________��
(4)H2D2B8��һ�־���ǿ�����ԵĶ�Ԫ��(���з��ӽṹ����2��Bԭ����-1��),��H2D2B8�ĽṹʽΪ___________�������в�ȡsp3�ӻ���Bԭ����______����
(5)E ���������ӵĶѻ�ģ����ͼ��ʾ��

��֪:E �������ܶ�Ϊ��g/cm3��NA���������ӵ�����ֵ��E �����ԭ������ΪM��
��E ���ӵ���λ��Ϊ_______��
��E ���Ӱ뾶Ϊ_______pm��
��E ���������ӵĿռ������ʦ�=_____(�ú��� ��ʽ�ӱ�ʾ)��
���𰸡� ![]() 3 O��S�۵�������ͬ�����ŵ��Ӳ��������࣬S��ԭ�Ӱ뾶����O������ԭ�Ӻ˶������ӵ����������� ��ԭ�Ӱ뾶����̼����ԭ�ӵ�ԭ�ӹ���粢���ص��̶�С���γɦ������ȶ�
3 O��S�۵�������ͬ�����ŵ��Ӳ��������࣬S��ԭ�Ӱ뾶����O������ԭ�Ӻ˶������ӵ����������� ��ԭ�Ӱ뾶����̼����ԭ�ӵ�ԭ�ӹ���粢���ص��̶�С���γɦ������ȶ�  (Ҳ��д��
(Ҳ��д��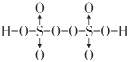 ) 4 12
) 4 12 ![]()
![]()
����������֪A��B��C��D��EΪԭ���������������ǰ������Ԫ����ǰ����Ԫ�صĻ�̬ԭ��p�ܼ�����2�������ӣ���AΪCԪ�ء�BΪOԪ�ء�CΪSiԪ�ء�DΪSԪ�أ�E��ԭ����������A��B��C����Ԫ��ԭ������֮�ͣ���E��ԭ������Ϊ��6+8+14��=28��EΪNiԪ�ء�
(1). E��NiԪ�أ�ԭ��������28����̬ԭ����Χ�����Ų�ʽΪ��3d84s2�����̬ԭ����Χ�����Ų�ͼΪ��![]() ��Niԭ�ӵ�M�ܲ���3s��3p��3d�����ܼ�������3��������ͬ�ĵ��ӣ��ʴ�Ϊ��
��Niԭ�ӵ�M�ܲ���3s��3p��3d�����ܼ�������3��������ͬ�ĵ��ӣ��ʴ�Ϊ��![]() ��3��
��3��
(2). O��SԪ�ش���ͬһ���壬����Ӳ��������࣬S��ԭ�Ӱ뾶����O������ԭ�Ӻ˶������ӵ�����������������OԪ�صĵ縺�Դ���S���ʴ�Ϊ��O��S�۵�������ͬ�����ŵ��Ӳ��������࣬S��ԭ�Ӱ뾶����O������ԭ�Ӻ˶������ӵ�������������
(3). ��̼Ԫ�صĻ������У�̼��ԭ��֮������γ�̼̼˫����̼̼������̼̼˫����̼̼�����ж����Цм������ԭ�Ӱ뾶����̼ԭ�ӣ���ԭ�ӵ�ԭ�ӹ���粢���ص��̶�С��̼ԭ�ӣ��γɵĦм����ȶ������Ժ���Ԫ�صĻ������У���ԭ�Ӽ�ֻ�ܴ����������ʴ�Ϊ����ԭ�Ӱ뾶����̼����ԭ�ӵ�ԭ�ӹ���粢���ص��̶�С���γɦм����ȶ���
(4). H2S2O8��һ�־���ǿ�����ԵĶ�Ԫ��������ӽṹ����2��Oԭ������1�ۣ�˵���÷��ӽṹ�к��й���������O��O������ϻ��ϼ۴�����Ϊ0����֪��ԭ����+6�ۣ�H2S2O8��һ�ֶ�Ԫ�ᣬ˵���÷��ӽṹ�к���2���ǻ�����H2S2O8�ĽṹʽΪ�� (Ҳ��д��
(Ҳ��д��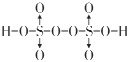 )���ɽṹʽ��֪���������е�������ԭ�Ӻ��ǻ��е�������ԭ�Ӳ�ȡsp3�ӻ������Բ�ȡsp3�ӻ���Oԭ����4�����ʴ�Ϊ��
)���ɽṹʽ��֪���������е�������ԭ�Ӻ��ǻ��е�������ԭ�Ӳ�ȡsp3�ӻ������Բ�ȡsp3�ӻ���Oԭ����4�����ʴ�Ϊ�� (Ҳ��д��
(Ҳ��д�� )��4��
)��4��
(5). ��. ��Ni���������ӵĶѻ�ģ��ͼ��֪��Ni���ӵ���λ��Ϊ3��8��2=12���ʴ�Ϊ��12��
��. Ni����������������������Խ���������Ni�������У���Ni�İ뾶Ϊr cm����������Ϊa cm�����ݹ��ɶ����ɵã�(4r)2=2a2��r =![]() a cm���ɾ�̯����֪��1��Ni�����к�4��Ni���ӣ����ܶ�
a cm���ɾ�̯����֪��1��Ni�����к�4��Ni���ӣ����ܶ�![]() =
=![]() ��a=
��a=![]() ��r =
��r = ![]() cm=pm���ʴ�Ϊ��
cm=pm���ʴ�Ϊ��![]() ��
��
��. ������Ni���ӵ���ĿΪ4������Ni�İ뾶Ϊr cm����������Ϊa cm�������������֪��Ni���Ӱ뾶Ϊ��r =![]() a cm����Ni�����ھ����еĿռ�������Ϊ��
a cm����Ni�����ھ����еĿռ�������Ϊ��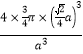 =
=![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��

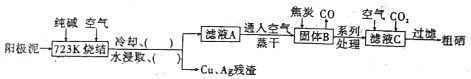
����Ŀ����֪Cr��OH��3�ڼ��Խ�ǿ����Һ�н�����[Cr��OH��4]�� �� ���Ļ������ж�������+6�۸���ǿ�����ԣ��䶾����+3�۸����Ե�100������ˣ�����Ժ����ķ�ˮ���д������ɲ����������ַ����� ������һ����ԭ�� �����Խ�������FeSO4�Ƚ�+6�۸���ԭ��+3�۸��������������£�![]()
�й�������ȫ������pH���±���
����� | Fe2+ | Fe3+ | Cr3+ |
��ȫ����Ϊ��Ӧ���������pH | 9.0 | 3.2 | 5.6 |
��1��д��Cr2O72����FeSO4��Һ�����������·�Ӧ�����ӷ���ʽ ��
��2����ԭ+6�۸�����ѡ�����µ��Լ�������ţ���
A.����
B.��м
C.��ʯ��
D.����������
��3���ں�����ˮ�м���FeSO4 �� �ٵ���pH��ʹFe3+��Cr3+��������������������ڲ������п����ڵ�����ҺpH���Լ�Ϊ��������ţ��� A��Na2O2 B��Ba��OH��2 C��Ca��OH��2
��ʱ������Һ��pH��Χ��������ţ���ѣ�
A��3��4 B��6��8 C��10��11 D��12��14
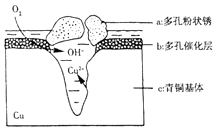
��4��������������ⷨ ����+6�۸��ķ�ˮ��������ڣ������������������������Ȼ��ƽ��е�⣮���������ɵ�Fe2+��Cr2O72һ������Ӧ�����ɵ�Fe3+��Cr3+����������OHһ�������Fe��OH��3��Cr��OH��3������ȥ�� д�������ĵ缫��Ӧʽ ��
��5����ⷨ�м����Ȼ��Ƶ������ǣ� ��