题目内容
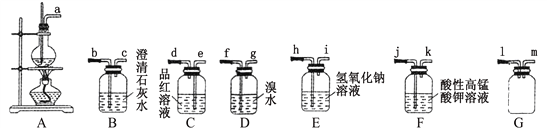
【题目】如图A为直流电源,B为浸泡饱和NaCl溶液和酚酞溶液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色。请填空:

(1)电源A上的a为_______ 极;
(2)滤纸B上发生的总化学方程式为_________________ ;
(3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e材料为_______ (写物质名称),电极f上发生的反应为____________,槽中盛放的电镀液可以是_______________,电镀液浓度 _________(不变、变大、变小)。
【答案】正 2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑ 锌 Zn2++2e-=Zn ZnSO4或Zn(NO3)2 不变
2NaOH+Cl2↑+H2↑ 锌 Zn2++2e-=Zn ZnSO4或Zn(NO3)2 不变
【解析】
(1)A为直流电源,B为浸泡饱和NaCl溶液和酚酞溶液的滤纸,由B上的c点显红色判断c的电极,根据c的电极判断a、b的电极类型;
(2)电解氯化钠溶液生成氯气、氢气和氢氧化钠,据此书写反应方程式;
(3)根据电镀原理分析解答。
(1)A为直流电源,B为浸泡饱和NaCl溶液和酚酞溶液的滤纸,B外接电源,所以B是电解饱和氯化钠溶液;B上的c点显红色,说明c点有氢氧根离子生成,根据离子的放电顺序知,该极上氢离子得电子放电,所以c是阴极,b是外电源的负极,a是正极,故答案为:正。
(2)电解氯化钠溶液生成氯气、氢气和氢氧化钠,反应方程式为 2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑,故答案为:2NaCl+2H2O
2NaOH+Cl2↑+H2↑,故答案为:2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑。
2NaOH+Cl2↑+H2↑。
(3)a为正极,电镀槽中,e是阳极,f是阴极,镀层锌作阳极,镀件铁作阴极,阳极的电极反应式为Zn-2e-=Zn2+,阴极的电极反应式为Zn2++2e-=Zn;选取含有镀层金属离子的溶液作电镀液,所以可选ZnSO4、Zn(NO3)2溶液作电镀液,电镀过程中,电镀液的浓度保持不变,故答案为:锌;Zn2++2e-=Zn; ZnSO4或Zn(NO3)2;不变。

 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案【题目】软锰矿的主要成分是MnO2,还含有少量金属铁、镁、铝、锌、铜的化合物等杂质。黄铁矿的主要成分是FeS2,还含有硅、铝的氧化物等杂质。工业上用软锰矿制备碳酸锰并回收硫酸铵,其主要流程如下:

已知金属离子从开始形成氢氧化物沉淀,到沉淀时溶液的pH如下表:
金属离子 | Fe2+ | Fe3+ | Al3+ | Cu2+ | Mn2+ |
开始沉淀pH | 7.5 | 2.7 | 4.1 | 5.9 | 8.8 |
完全沉淀pH | 9.5 | 3.7 | 5.4 | 6.9 | 10.8 |
(1)提高浸出率的可采取的措施有____。
a.适当升高温度 b.搅拌 c.加适量纯碱 d.加压
(2)浸取完成后,取浸取液少许,加入KSCN溶液无明显现象,则浸取时发生的主要反应的化学方程式是__________________________。
(3)调节pH为5.4~5.8的目的是______________。
(4)滤渣3的主要成分的化学式是_______。
(5)采用50℃碳化的原因是_________________________________。该过程发生反应的离子方程式是__________________。
(6)检验碳酸锰产品完全洗净的方法是_______________________________。
【题目】现有部分短周期元素的性质或原子结构如表所示:
元素编号 | 元素性质或原子结构 |
X | 其简单离子在第3周期元素的简单离子中半径最小 |
Y | 其最简单氢化物丙的水溶液呈碱性 |
Z | 原子核外电子数和周期序数相等 |
A、B、D三种单质(单质分别由X、Y、Z元素组成)和甲、乙、丙、丁、戊五种化合物之间的转化关系如图所示(某些条件已略去)。其中丁是一种火箭发动机的高能燃料,一个分子中含有18个电子,其组成元素与丙相同,戊是两性氢氧化物。
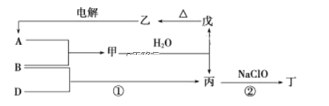
请回答:
(1)元素X在周期表中的位置是________,其简单离子的结构示意图为________。
(2)单质B电子式为________、丁电子式为________。
(3)丙中所包含的化学键类型有_______(填字母序号)。
a.离子键 b.极性共价键 c.非极性共价键
(4)反应②中,1 mol NaClO参加反应时,转移2 mol电子,其离子方程式为______________。
(5)一定条件下,A与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。该化学方程式为____________________。