题目内容
14.在298K时,实验测得溶液中的反应H2O2+2HI═2H2O+I2在不同浓度时的化学反应速率见表:反应H2O2+2HI═2H2O+I2在不同浓度时的化学反应速率
| 实验编号 | 1 | 2 | 3 | 4 | 5 |
| c(HI)/mol•L-1 | 0.100 | 0.200 | 0.300 | 0.100 | 0.100 |
| c(H2O2)/mol•L-1 | 0.100 | 0.100 | 0.100 | 0.200 | 0.300 |
| ν(HI)/mol•L-1•s-1 | 0.00760 | 0.0153 | 0.0227 | 0.0151 | 0.0228 |
(2)上式表达式中κ称为速率常数,通常情况下,κ越大,反应进行的越快.
分析 根据表中数据可知,速率与c(HI)成正比、与c(H2O2)成正比,据此写出此反应的速率方程,速率常数随催化剂、固体表面性质等因素的影响,K越大速率越快;
解答 解:(1)当c(HI)=0.100mol•L-1,c(H2O2)=0.100mol•L-1,υ=0.00760mol•L-1•s-1,c由表中数据可知,速率与c(HI)成正比、与c(H2O2)成正比,反应的速率方程为v=Kc(HI)c(H2O2),
故答案为:v=Kc(HI)c(H2O2);
(2)速率方程为:v=Kc(HI)c(H2O2),Kc为速率常数,它表示单位浓度下的化学速率,与浓度无关,但受温度、催化剂、固体表面性质等因素的影响,K越大反应进行越快,
故答案为:速率常数,越快.
点评 本题考查化学反应速率的定量表示方法,题目难度不大,可对三组数据比较计算,掌握数据分析方法是解题关键.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
4.向硝酸钡溶液逐渐通入二氧化硫气体,可能发生的离子方程式如下,其中错误的是( )
| A. | 3SO2+2NO3-+2H2O═2NO↑+4H++3SO42- | |
| B. | 3SO2+Ba2++2NO3-+2H2O═BaSO4↓+2NO↑+4H++SO42- | |
| C. | 6SO2+Ba2++4NO3-+4H2O═BaSO4↓+4NO↑+8H++5SO42- | |
| D. | 3SO2+3Ba2++2NO3-+2H2O═3BaSO4↓+2NO↑+4H+ |
5.下列根据实验操作和实验现象所得出的结论不正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向沸水中滴加少量饱和氯化铁溶液,加热至溶液呈红褐色,用激光笔照射 | 有丁达尔效应 | 红褐色液体为胶体 |
| B | 向溶液X中加入NaHCO3粉末 | 产生无色气体 | X一定属于酸 |
| C | 向淀粉NaI溶液中加入氯水 | 溶液变蓝 | 氧化性:Cl2>I2 |
| D | 将气体X分别通入溴水和酸性高锰酸钾溶液 | 两溶液均褪色 | X可能是SO2 |
| A. | A | B. | B | C. | C | D. | D |
9.用NA表示阿佛加德罗常数,下列说法正确的是( )
| A. | 标准状况下,2.24L水所含的分子数目为0.1 NA | |
| B. | 9g水中含有的电子数目为0.5NA | |
| C. | 0.3 mol/L的MgCl2溶液中含Mg2+数目为0.3 NA | |
| D. | 常常压下,28gN2和CO混合气体中所含有的原子数目为2NA |
19.下列有关物理量相应的单位表达中,错误的是( )
| A. | 摩尔质量g/mol | B. | 气体摩尔体积L/mol | ||
| C. | 溶解度g/10g | D. | 密度g/cm3 |
6.在无色溶液中下列各组离子能大量共存的是( )
| A. | Ag+、K+、NO${\;}_{3}^{-}$、Cl- | B. | Mg2+、Na+、Cl-、SO${\;}_{4}^{2-}$ | ||
| C. | Ca2+、Mg2+、Fe2+、Cl- | D. | H+、Na+、CO${\;}_{3}^{2-}$、SO${\;}_{4}^{2-}$ |
4.化学与生产、生活密切相关.下列说法不正确的是( )
| A. | 闻名世界的中国陶瓷、酿酒、造纸技术都充分应用了化学工艺 | |
| B. | 四大发明之一黑火药是由硫黄、硝石、木炭三种物质按一定比例混合制成 | |
| C. | 侯氏制碱法的工艺过程中应用了物质溶解度的差异 | |
| D. | 打磨磁石制作指南针为化学变化 |

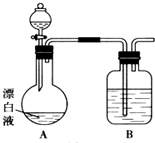 某化学兴趣小组同学看到一则报道:某造纸厂误将槽车中漂白液(NaCl和NaClO的混合液)倒入盛放饱和KAl(SO4)2溶液的池中,造成中毒事件.该小组同学为探究中毒原因进行了如下实验.
某化学兴趣小组同学看到一则报道:某造纸厂误将槽车中漂白液(NaCl和NaClO的混合液)倒入盛放饱和KAl(SO4)2溶液的池中,造成中毒事件.该小组同学为探究中毒原因进行了如下实验.